Dieser Artikel ist schon länger nicht mehr aktualisiert worden und spiegelt nicht mehr zuverlässig den aktuellen Stand von Wissen und Nichtwissen - für tagesaktuelle Infos schauen Sie bitte in den blog unter coronoia.info.
Schon früh in der COVID-19-Pandemie tauchte in der öffentlichen Diskussion der Begriff der "Herdenimmunität" auf, oft mit willkürlich behaupteten, stark von einander abweichenden Prozentangaben von Menschen, die gegen die Erkrankung immun sein müssten, damit die Pandemie endlich zu Ende...
Was ist denn eigentlich eine Herdenimmunität?
{slider Delta und die Herde - Zusammenfassung vom 07.08.2021}
Dieses Video vom 28.07.2021 fasst auch am 07.08. die Situation im wesentlichen zusammen
Inzwischen hat sich die Situation allerdings noch dahingehend geklärt, dass die US-amerikanischen CDC mittlerweile kurz und knapp zusammenfassen [Hervorhebungen von mir]:
"Our vaccines are working exceptionally well," so Rochelle Walensky gegenüber CNN "They continue to work well for Delta, with regard to severe illness and death -- they prevent it. But what they can't do anymore is prevent transmission." (cnn 05.08.2021)
Rochelle Walensky ist die Chefin der CDC - die US-amerikanische Lothar Wieler...
So knapp können wohl nur die Amerikaner ein komplettes Programmpaket an Pandemiemaßnahmen zusammenfassen bzw. zusammenstreichen:
-
wer immer sich (vorübergehend, s. hier) vor schweren Verläufen und Tod an COVID-19 schützen will, kann dies tun und sich impfen lassen (ggf. alle 3 Monate) - alle anderen haben damit nichts mehr zu tun....
-
Jede Idee an eine "Herdenimmunität", jeder Gedanke an eine wie hoch auch immer angesiedelte "Durchimpfungsrate" ist mit diesem résumée der CDC once and for all ad absurdum geführt - es geht nur und allein um den (begrenzt möglichen) Eigenschutz. Mehr können die Impfstoffe einfach nicht. Period.
In England ist dies offenbar schon länger bekannt, spätestens seit der Sitzung des SAGE, einem Krisenstab von Public Health England, der schon auf seiner Sitzung am 22.07. feststellte:
"33. ONS data suggest that for those who have been vaccinated who do get infected with the delta variant, PCR cycle threshold (Ct) values are generally lower than for those infected with alpha, suggesting that vaccinated people may still have a high viral load with delta infection (medium confidence). This may mean that there is limited vaccine effect against on onward transmission for the delta variant." [immer daran denken: je niedriger der Ct-Wert, desto ansteckender, nicht wahr, liebe Frau Merkel?]
Ninety-fourth SAGE meeting on COVID-19, 22 July 2021
{/sliders}
{slider Vorbemerkung: "Am Anfang war das Wort..."}
Die Geschichte des Begriffs der "Herdenimmunität", die im humanmedizinischen Bereich im Anfang des 20. Jahrhunderts beginnt, ist von Anfang an eine Geschichte von Missverständnissen und willkürlichen (Teil-)Definitionen, wie Fine in zwei wesentlichen Arbeiten 1993 und 2011 feststellt:
"The term ‘‘herd immunity’’ is widely used but carries a variety of meanings […]. Some authors use it to describe the proportion immune among individuals in a population. Others use it with reference to a particular threshold proportion of immune individuals that should lead to a decline in incidence of infection. Still others use it to refer to a pattern of immunity that should protect a population from invasion of a new infection. A common implication of the term is that the risk of infection among susceptible individuals in a population is reduced by the presence and proximity of immune individuals (this is sometimes referred to as ‘‘indirect protection’’ or a ‘‘herd effect’’)" [Der Begriff der "Herdenimmunität" ist weit verbreitet und trägt eine Vielzahl von Bedeutungen [Literaturzitate in der Originalarbeit]. Einige Autoren nutzen ihn, um den Anteil Immuner in einer Bevölkerung zu beschreiben. Andere verwenden ihn mit Bezug auf einen definierten Anteil immuner Individuen, der zu einer Abnahme der Inzidenz einer Infektion führen solle. Wieder andere nutzen ihn hinsichtlich eines Immunitätsmusters, das eine Bevölkerung vor dem Ausbrechen einer neuen Infektionskrankheit schützen solle. Eine übliche Bedeutung des Begriffs ist, dass das Risiko der Infektion für empfängliche Individuen in einer Bevölkerung durch das Vorhandensein immuner Individuen verringert wird (dies wird manchmal auch als "indirekter Schutz" oder "Herdeneffekt" bezeichnet.] (Fine 2011).
Von wirklicher epidemiologischer Relevanz sind zwei (Teil-)Aspekte der Herdenimmunität:
-
zum einen, dass in einer Bevölkerung so viele Menschen immun sind, dass jemand, der für diese Erkrankung ansteckend ist, auf so wenige Nicht-Immune trifft, dass er im Durchschnitt weniger als eine weitere Person ansteckt (die effektive Reproduktionszahl R wäre damit kleiner als 1 und eine Epi/Pandemie käme zum Erliegen (s. hier). Für diesen Aspekt der Herdenimmunität ist eine "sterile Immunität", die die Weitergabe der Erkrankung durch Immune verhindert, nicht zwingend erforderlich.
-
zum anderen, dass Nicht-Immune in einer Bevölkerung dadurch geschützt werden, dass sie im Wesentlichen von Immunen umgeben sind, die aufgrund der eigenen Immunität die Erkrankung auch nicht mehr weitergeben. Unabdingbare Voraussetzung für dieses Verständnis der Herdenimmunität ist natürlich, dass die Immunität des/der Einzelnen nicht nur vor der eigenen Erkrankung schützt, sondern auch vor der Weitergabe des Krankheitserregers an andere ("sterile Immunität").
Dieser letzten Bedeutung - den Schutz grundsätzlich Empfänglicher vor Ansteckung durch die Immunität der anderen - schließen sich heute die Mehrzahl der fachkundigen Autoren und auch die Gesundheitsbehörden an (Hervorhebung von mir):
-
"Herdenschutz (engl.: heard immunity) Herdenimmunität; der Effekt, dass ein gewisser Anteil immuner Individuen innerhalb einer Population (entstanden durch Impfung oder abgelaufene Infektionen) auch nichtimmunen Personen einen relativen Schutz bietet" (RKI 2015 - Rechtschreibfehler heard (eigentlich: herd) im Original)
- Community immunity: A situation in which a sufficient proportion of a population is immune to an infectious disease (through vaccination and/or prior illness) to make its spread from person to person unlikely. Even individuals not vaccinated (such as newborns and those with chronic illnesses) are offered some protection because the disease has little opportunity to spread within the community. Also known as herd immunity. (CDC 2020).
{slider Herdenimmunität nach der COVID-19-Erkrankung}
Eine große Studie der englischen Gesundheitsbehörden PHE konnte darüber hinaus nachweisen, dass nicht einmal eine durch die durchgemachte Erkrankung erworbene Immunität die Übertragung von COVID-19 auf Andere verhindert
"PHE also warned that although those with antibodies have some protection from becoming ill with COVID-19 themselves, early evidence from the next stage of the study suggests that some of these individuals carry high levels of virus and could continue to transmit the virus to others." (PHE 2021, Originalstudie Hall 2021).
Eine weitere Studie aus Südafrika stellt die Herdenimmunität durch "Durchseuchung" angesichts der zeitlich befristeten Immunität nach der Erkrankung und der zunehmend auftauchenden Mutationen (VOCs/variants of concern) in Frage: in Südafrika haben in einigen Regionen offenbar mehr als 60% der Menschen COVID-19 (ganz überwiegend unbemerkt) durchlebt - dennoch gibt es unverändert hohe Neuinfektionszahlen. "As has been seen in other areas, even such high seroprevalence does not guarantee population-level immunity against new outbreaks – probably due to viral evolution and waning of antibody neutralization" (Sykes 2021 - preprint).
Ähnliche Zahlen gibt es aus Manaus in Brasilien: hier zeigte eine Studie nach der "ersten Welle" Antikörper bei bis zu 76% der Blutspender (Buss 2020 - preprint) - dennoch leidet Manaus (vor allem auch durch die VOC P.1) derzeit an einer massiven "zweiten Welle" mit hohen Zahlen von Todesfällen (Taylor 2021 - preprint).
Auch wenn Daten von Blutspendern sicher nicht bevölkerungsrepräsentativ sind, gehen Experten z.B. der Havard-University nicht davon aus, dass die tatsächlichen Antikörper-Prävalenzen in der Bevölkerung in völlig anderen Dimensionen lägen (“It’s possible that the modelling is wrong, and seroprevalence (the amount of antibodies measured in the blood serum as a marker of pathogen exposure, used to estimate the proportion of the population that has been infected) in people is actually lower, ” so William Hanage, ein Epidemiologe in Harvard. “But I don’t think it’s possible that they were that much lower.” (Taylor 2021)
Damit bleibt es derzeit völlig offen, ob COVID-19-Erkrankung oder -Impfung eine Herdenimmunität erzeugen können, die die Übertragung der Erkrankung auf Nicht-Immune relevant vermindert.
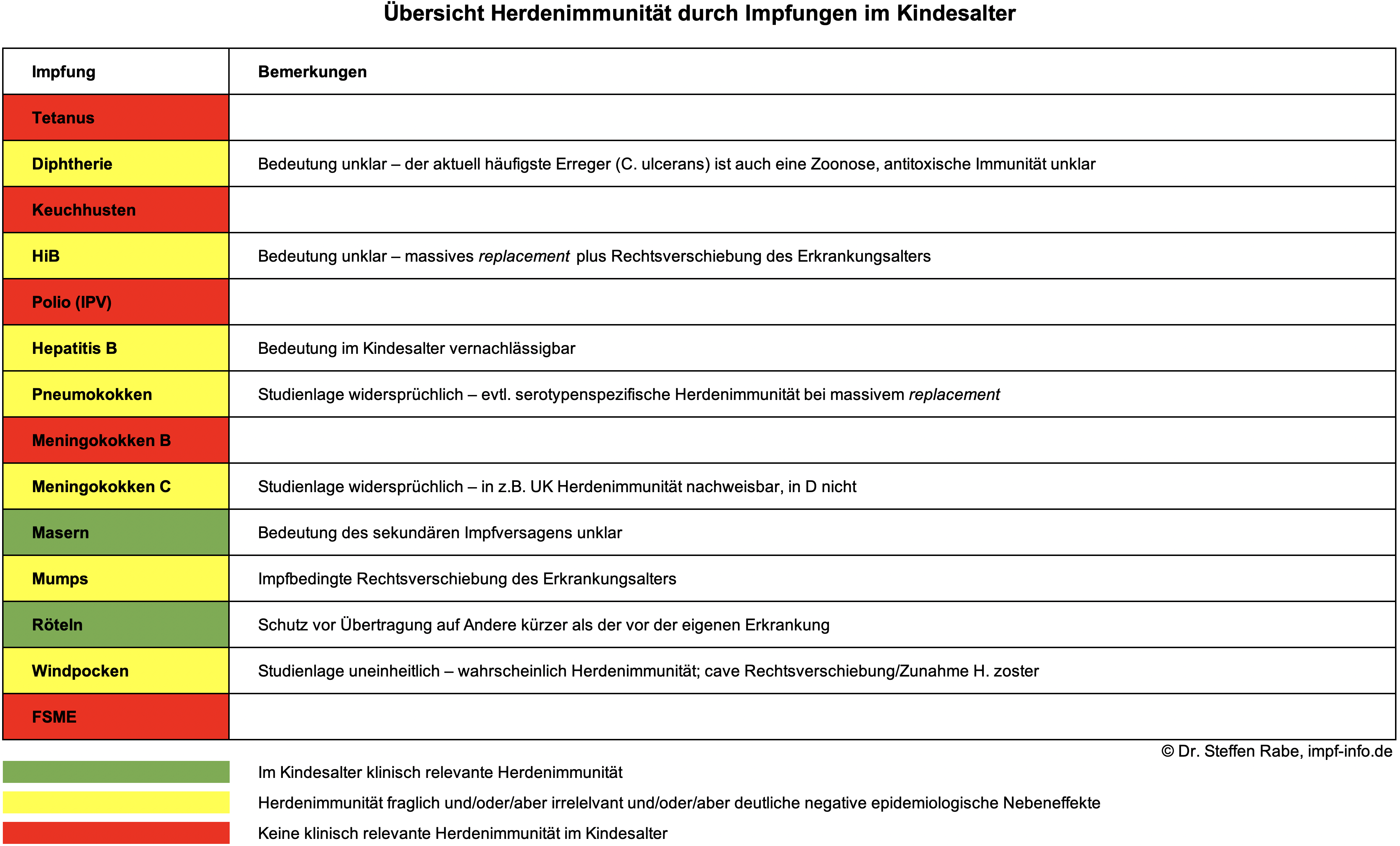
{slider Herdenimmunität durch Impfungen - Allgemein}
Der Schutz der Gemeinschaft durch die Impfung des/der Einzelnen ist zwar eine oft unausgesprochene gedankliche Prämisse bei und nicht selten ein klassisches Totschlagargument in Diskussionen über Impfungen, tatsächlich erzeugen aber schon von den etablierten Impfstoffen nur sehr wenige eine klinisch bedeutsame Herdenimmunität. Eine kurze Übersicht finden Sie hier, ausführlicher ist das Thema hier erläutert:
{slider Herdenimmunität durch COVID-19-Impfstoffe}
{slider-1 Vorbemerkung}
Auch bei COVID-19 versteht das Robert Koch-Institut den Begriff Herdenimmunität fraglos im Sinne der fehlenen Übertragbarkeit der Erkrankung:
"Je nachdem, in welchem Maße die COVID-19-Schutzimpfung Übertragungen verhindert, können immune Mitglieder der Gemeinschaft die Infektionsketten brechen, und nicht-immune Mitglieder schützen. Man spricht dann von Gemeinschaftsschutz („Herdenimmunität“)." (RKI 2021)
Die Frage, ob alle oder einzelne der mittlerweile zugelassenen Impfstoffe dies vermögen, ist derzeit noch offen: die STIKO schreibt hierzu in der 3. Aktualisierung der COVID-19-Impfempfehlung:
"Die bisher vorliegenden Daten erlauben nicht, die Wirksamkeit der mRNA- und Vektor-basierten COVID-19-Impfstoffe hinsichtlich einer Verhinderung der Transmission abschließend zu bewerten. Allerdings kann eine Verminderung der Virusausscheidung bei nach Impfung Infizierten als gesichert angesehen werden." (STIKO 2021).
In der mittlerweile vorliegenden 4. Aktualisierung heißt es: "Auf Basis der bisher vorliegenden Daten ist anzunehmen, dass die Virusausscheidung bei nach vollständiger Impfung Infizierten stark reduziert ist und damit das Risiko der Transmission vermindert ist. Es muss jedoch davon ausgegangen werden, dass Menschen nach Kontakt mit dem Virus (Exposition) trotz Impfung symptomatisch oder asymptomatisch infiziert werden können und dabei das Virus SARS-CoV-2 ausscheiden (nachgewiesen durch PCR-Testung). Deshalb sollten auch nach Impfung die allgemein empfohlenen Schutzmaßnahmen weiterhin eingehalten werden." (STIKO 2021b) - die STIKO geht also unverändert grundsätzlich von einer möglichen Infektiosität auch vollständig Geimpfter aus.
{slider-1 Comirnaty® von BioNTech}
Daten aus Israel, das seine forcierte Impfstrategie vor allem mit dem Impfstoff von BioNTech umsetzte, zeigen, dass die Ct-Werte positiver PCR-Test in der Bevölkerungsgruppe der über 60-Jährigen verglichen mit denen der 40 - 60-Jährigen parallel zur Impfkampagne anstiegen (und damit die Viruslast sank). Da die ältere Bevölkerungsgruppe die primäre Zielgruppe der Impfung war, wird dies als Hinweis auf eine möglicherweise reduzierte Viruslast und damit eine möglicherweise reduzierte Infektiosität in der am stärksten geimpften Bevölkerungsgruppe als Effekt der Impfung interpretiert (Guardian 09.02.2021, Erlich 2021 - preprint) - ob dieser bis jetzt bloßen Koinzidenz (weniger Viruslast bei denen, von denen mehr geimpft sind) aber tatsächlich ein kausaler Zusammenhang (weniger Viruslast, weil von dieser Gruppe mehr geimpft sind) zu Grunde liegt, ist derzeit noch offen.
Eine zweite Arbeit aus Israel fand bei Neuinfektionen 12 Tage nach der Impfung eine signifikant geringere Viruslast verglichen mit Neuinfektionen Ungeimpfter (Levine-Tiefenbrun 2021 - preprint) - auch dies könnte auf eine geringere Infektiosität nach der Impfung hinweisen. "Allerdings hat die Studie einige Einschränkungen: So bleibt laut Marco Binder vom Deutschen Krebsforschungszentrum in Heidelberg fraglich, inwieweit sich eine vierfache Verringerung in Anbetracht der typischerweise nachgewiesenen RNA-Mengen im Bereich von Hunderttausenden oder Millionen von RNA-Molekülen tatsächlich auf die Infektiosität auswirkt. Auch spielen hierfür die Viren aus dem Rachen eine grössere Rolle als jene aus der Nase – in der Studie wurden jedoch Proben aus Nasen-Rachen-Abstrichen untersucht, worauf auch die Autoren hinweisen. Ebenfalls unklar ist, wie sich der gemessene Effekt über die Zeit entwickelt. Zudem wird die verwendete Methode als für diesen Zweck zu ungenau kritisiert." (NZZ 12.02.2021)
Eine besondere Bedeutung kommt der SIREN-Studie des englischen Gesundheitssystems Public Health England (PHE) zu (Hall 2021a):
hier wurden über Monate Beschäftigte im Gesundheitswesen mit oder ohne COVID-19-Infektion in der Vorgeschichte in regelmäßigen Abständen mit PCR- und Antikörpertests auf COVID-19-(Re-)Infektionen untersucht und dies unabhängig von eventuell auftretenden Symptomen. Dadurch ermöglicht diese Untersuchung erstmals auch belastbare Aussagen über asymptomatische SARS-CoV-2-Infektionen bei Geimpften oder Ungeimpften. Im Studienverlauf wurde die Mehrzahl der Probandinnen und Probanden geimpft, ganz überwiegend (94%) mit dem BioNTECH-Impfstoff, 6% erhielten das AstraZeneca-Präparat.
Es ergab sich für jede Form von SARS-CoV-2-Infektion (also symptomatische und asymptomatische*) eine Effektivität des Impfstoffs von 70 (nach der ersten Impfdosis) bis 85% (nach der zweiten Impfdosis) und es zeigte sich, dass auch die asymptomatischen Infektionen bei Geimpften seltener nachzuweisen waren als bei Ungeimpften. Dies wird von den Autoren der Studie (und vor allem von den Medien...) als Beweis für eine Verringerung des Übertragungsrisikos und damit für eine entstehende Herdenimmunität durch die Impfung gewertet (da für eine Übertragung ja zumindest eine asymptomatische Infektion vorliegen muss). Auch wenn dies grundsätzlich richtig ist, muss folgendes beachtet werden:
-
das Auftreten asymptomatischer SARS-CoV-2-Infektionen wurde durch die Impfung(en) zwar verringert, aber keineswegs verhindert - damit ist eben auch nachgewiesen, dass auch Geimpfte sich weiterhin unbemerkt infizieren und die Infektion weiterverbreiten können, es kann also im günstigsten Fall ein begrenzter Herdenschutz durch die Impfung angenommen werden (wenn sich diese Daten in weiteren Studien bestätigen)
-
und auch wenn die geringen absoluten Zahlen der nachgewiesenen asymptomatischen Infektionen (51 bei Ungeimpften, 10 bei Geimpften) eine prozentuale Betrachtung problematisch machen: der jeweilige Anteil asymptomatischer Infektionen an den insgesamt nachgewiesenen Infektionen ist bei Geimpften doppelt so hoch gewesen, wie in der ungeimpften Gruppe. Dies könnte bedeuten, dass das Risiko, dass eine SARS-CoV-2-Infektion nach Impfung asymptomatisch und damit unbemerkt verläuft, höher ist. Sollten sich diese Daten bestätigen, liegt hierin das Risiko, dass Geimpfte aufgrund der fehlenden Symptomatik (und des ohnehin subjektiven Gefühls, eigentlich durch die Impfung geschützt zu sein) bei einer Infektion keine Vorsichtsmaßnahmen ergreifen und daher doch relevant zu Weiterverbreitung beitragen (ein Phänomen, wie wir es von der Keuchhustenimpfung kennen).
Eine weitere Studie der Universitätskliniken in Cambridge weist in die selbe Richtung, wirft aber mehr Fragen auf, als dass sie Antworten lieferte (Weekes 2021 - preprint). Auch hier wurden Mitarbeiter im Gesundheitssystem (HCWs für health care workers) regelmäßig per PCR untersucht, Ziel der Studie war der Nachweis "asymptomatischer Infektionen"*. Es wurden vergleichbar große Zahlen ungeimpfter und geimpfter HCWs untersucht, letztere differenziert nach dem Zeitraum von weniger als 12 Tagen nach der Impfung und ab dem 12. Tag nach der Impfung (in den bisherigen Studien fand sich ein nachweisbarer Effekt auf COVID-19-Erkrankungen immer erst ab etwa dem 12. Tag nach der Impfung/post vacc.).
-
bei den Ungeimpften fanden sich 0,8% positive PCRs bei HCWs, die sich "well to work" fühlten
-
bei den Geimpften "well to work" fanden sich 0,37% positive PCRs in dem Zeitraum < 12 Tage post vacc. und 0,2% in dem Zeitraum ≥ 12 Tage post vacc. - hieraus errechnen die Studienautoren eine Effektivität von 75% in der Reduktion "asymptomatischer Infektionen"*/Kolonisationen verglichen mit den 0,8% in der Ungeimpften Gruppe.
- hier liegt jedoch ein gedanklich-methodischer lapsus vor: die Studienautoren selber wählen den Zeitpunkt von 12 Tagen nach der Impfung als vermeintlichen (und biologisch durchaus plausiblen) Wirkbeginn der Impfung, abgelesen aus den Zulassungsstudien. Damit kann dann aber der auffallende Unterschied zwischen Ungeimpften und Geimpften vor diesem Zeitpunkt (0,8% vs. 0,37%) nicht ohne weiteres der Tatsache der Impfung zugeschrieben werden, sondern hier sind andere Ursachen, die in der Studie nicht berücksichtigt wurden, als möglich Erklärung näherliegend (so genannte confounder). Die einzig sicher nachgewiesene Reduktion "asymptomatischer Infektionen"*/Kolonisationen durch die Impfung wäre demnach nicht 0,8% auf 0,2%, sondern lediglich 0,37% auf 0,2%... was weitaus weniger spektakulär ist...
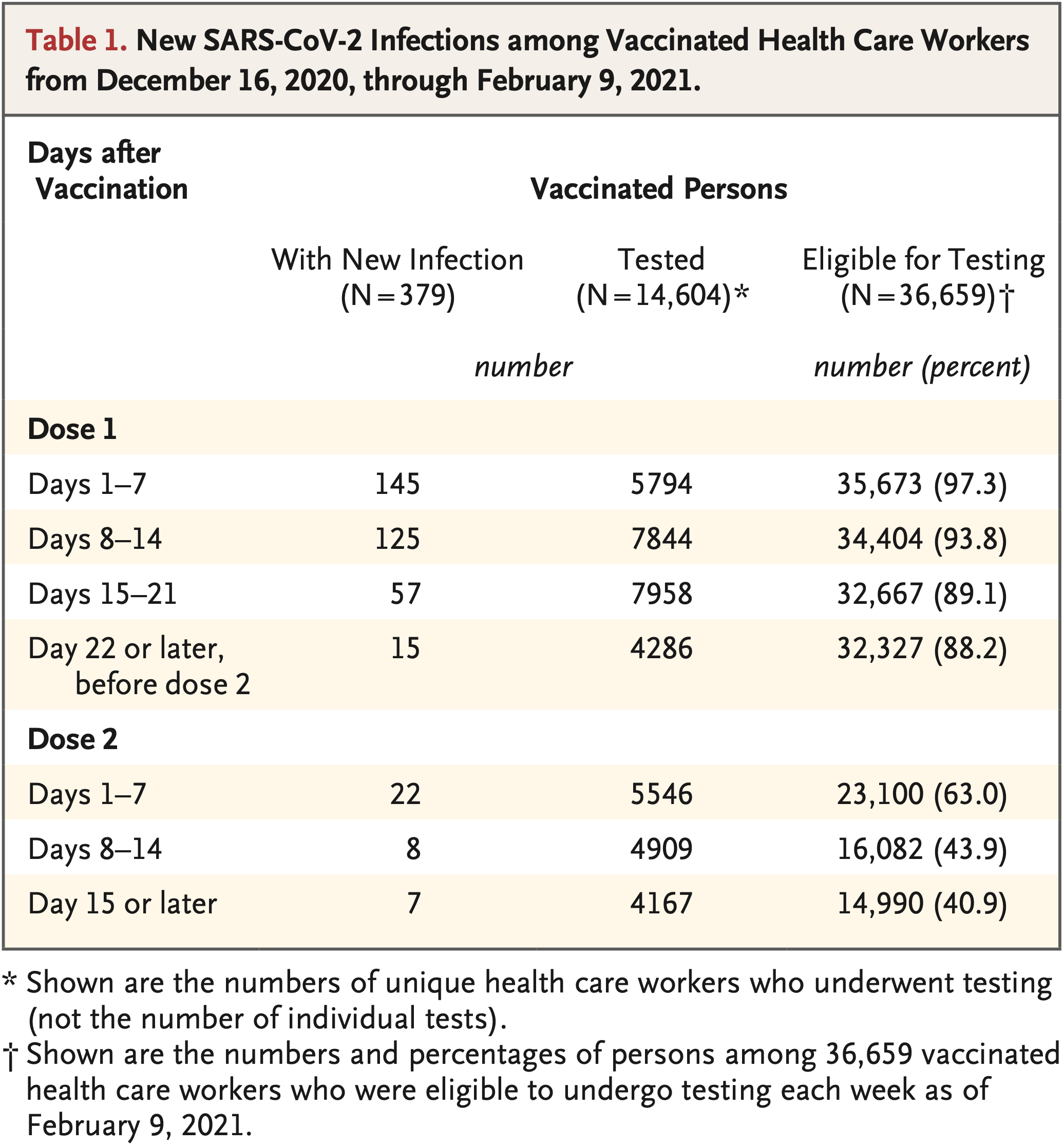
Eine Studie der amerikanischen CDC an HCWs des Netzwerkes HEROES-RECOVER (Thompson 2021) wird derzeit als weiterer Beweis für die Verminderung auch asymptomatischer Infektionen (und damit des Übertragungsrisikos) durch die Impfung in den Medien zitiert (z.B. tagesschau 29.03.2021) - wohl wegen des (absichtlich?) missverständlichen Satzes "These findings indicate that authorized mRNA COVID-19 vaccines are effective for preventing SARS-CoV-2 infection, regardless of symptom status, among working-age adults in real-world conditions.". Dieser wird in dem Sinne interpretiert, dass die errechnete Impfeffektivität bei asymptomatischen* und symptomatischen Infektionen gleich stark ausgeprägt sei - genau diese Aussage lässt die Studie allerdings nicht zu:
-
untersucht wurden 3950 HCWs von denen im Studienzeitraum 477 einmal, 2479 zweimal geimpft wurden und 994 ungeimpft blieben - verwendet wurden die Impfstoffe von BioNTech und Moderna
-
alle Teilnehmer wurden wöchentlich unabhängig von eventuellen Symptomen und zusätzlich bei Auftreten COVID-19-verdächtiger Symptome einer PCR unterzogen ("routinely tested for SARS-CoV-2 infections every week regardless of symptom status and at the onset of symptoms consistent with COVID-19–associated illness")
-
insgesamt wurden 205 positive PCR-Tests gefunden, von denen 87,3% von COVID-19-typischen, 2% von COVID-19-untypischen und 10,7% von keinerlei Symptomen begleitet wurden
-
aus der Gesamthäufigkeit positiver PCR-Tests und ihrer Verteilung auf Geimpfte und Ungeimpfte werden die bekannten Impfeffektivitäten von etwa 80% nach einer und 90% nach zwei Impfdosen errechnet
-
in den veröffentlichten Studienunterlagen findet sich überhaupt kein Hinweis darauf, wie sich die symptomatischen und die asymptomatischen* Infektionen auf die Geimpften und Ungeimpften verteilen, so dass völlig offen ist, ob und in welchem Umfang die reine Besiedlung durch die Impfungen verringert wird. (Theoretisch könnten ja alle 22 asymptomatischen Fälle bei Geimpften aufgetreten sein - die Studie schweigt sich hierzu aus.) "Regardless of symptom status" bezieht sich also ausschließlich auf die anlasslose Routinetestung, nicht auf die Impfstoffeffektivität. Bei der Effektivität meint "regardless" nur: das haben wir nicht angeschaut...
Eine Studie der kalifornischen Universitäten von San Diego (UCSD) und Los Angeles (UCLA) bei mit mRNA-Impfstoffen geimpften asymptomatischen HCWs fand ein absolutes Risiko positiver PCR-Tests nach Impfung von etwa 1% ("In our cohort, the absolute risk of testing positive for SARS-CoV-2 after vaccination was 1.19% among health care workers at UCSD and 0.97% among those at UCLA") (Keehner 2021). Selbst mehr als 2 Wochen nach der zweiten Impfung wurden noch mit SARS-CoV-2 besiedelte und damit potentiell infektiöse HCWs gefunden:
Die bisher mit Abstand aussagekräftigste Studie zur Frage des Übertragungsrisikos nach Impfung stammt von Public Health England (Harris 2021): hier wurden in mehr als 300.000 Haushalten das Risiko verglichen, sich bei einem infizierten Haushaltsmitglied ("index case") anzustecken, wenn dieses entweder ungeimpft war oder mindestens 21 Tage zuvor entweder Vaxzevria® oder Comirnaty® erhalten hatte. Das Ergebnis ist ernüchternd: "These results show that the likelihood of household transmission is 40-50% lower for households in which the index cases are vaccinated 21 days or more prior to testing positive (compared to no vaccination), with similar effects for both ChAdOx1 nCoV-19 and BNT162b2 vaccines." - das Risiko der Übertragung auf andere wurde nicht einmal halbiert...
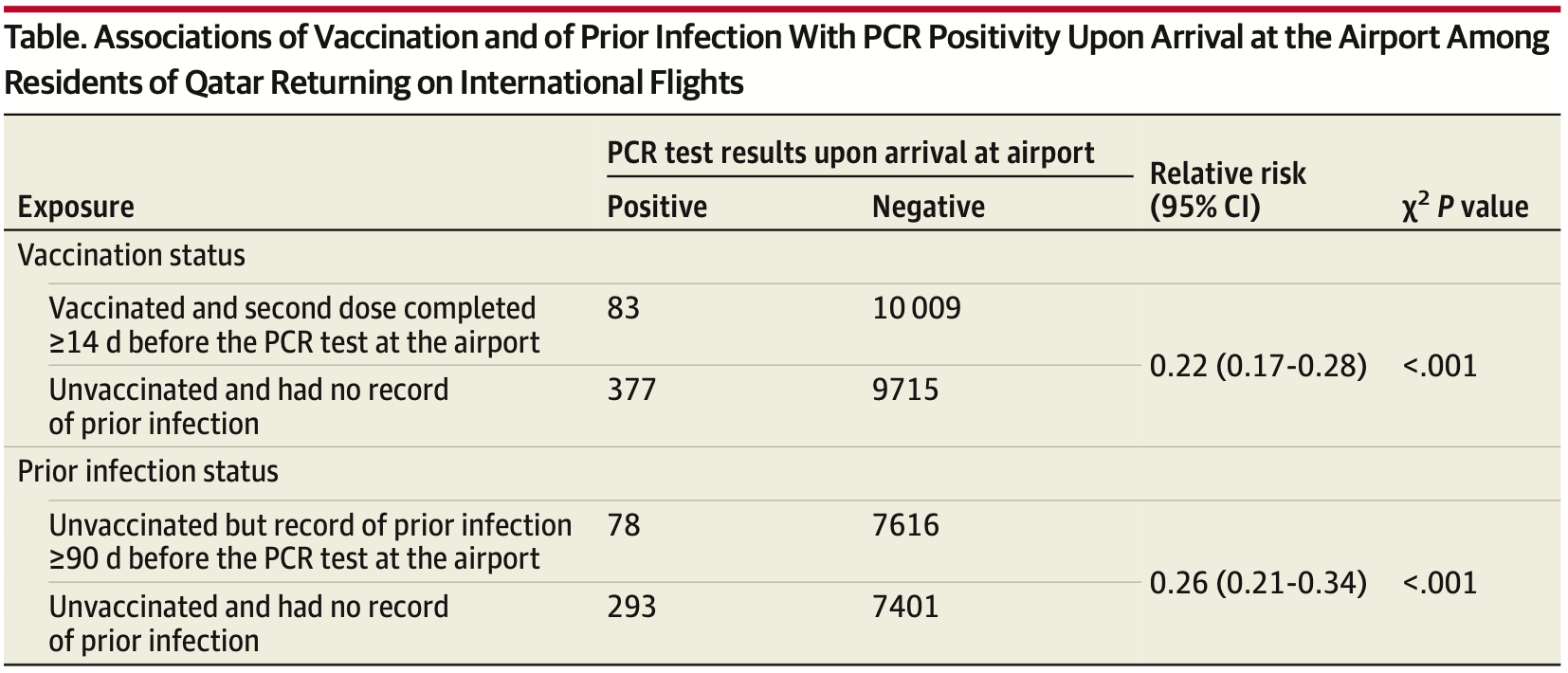
Eine große Studie des Flughafens in Qatar korrelierte PCR-Abstriche bei ankommenden Reisenden (> 75% Männer) mit vorangegangenen Impfungen (BioNTech oder Moderna, 2. Impfdosis ≥ 14 Tage vor dem Abstrich) oder COVID-19-Erkrankungen. Es zeigte sich, das sowohl die vollständige Impfung, als auch die anamnestische Erkrankung das Risiko eines positiven PCR-Befundes deutlich verminderte:
Die Studie zeigt aber auch, dass selbst nach zweimaliger Impfung ein relevantes Risiko für eine Neubesiedlung besteht und sie hat die deutliche methodische Schwäche, dass die jeweiligen Kontrollgruppen rein anamnestisch definiert sind. Gerade in der Gruppe der untersuchten jungen Männer (medianes Alter 33 Jahre) verlaufen viele SARS-CoV-2-Infektionen a- oder oligosymptomatisch und sind damit als solche nicht erinnerlich - dies verfälscht die Zusammensetzung und damit die Befunde der Kontrollgruppen in unkalkulierbarer Art und Weise (Bertollini 2021).
(* eine "asymptomatische Infektion" ist streng genommen natürlich keine Infektion, sondern lediglich eine Besiedlung/Kolonisation - auch diese kann jedoch zur Übertragung des Erregers führen; die Begriffe werden in den aktuellen Arbeiten nicht sauber getrennt verwendet)
{slider-1 mRNA-1273 von Moderna}
in den Zulassungsstudien wurde diese Fragestellung schlicht nicht untersucht (Doshi 2020) - lediglich bei einer der Studien zum mRNA-1273 von Moderna wurde im Verlauf ein PCR-Kontrollabstrich durchgeführt:
"Ein routinemäßig durchgeführter Abstrich aus dem Nasenrachenraum zum Zeitpunkt der 2. Impfung ergab, dass in der Plazebogruppe 39 und in der Verumgruppe 15 Personen PCR-positiv waren für SARS-CoV-2 (0,3 vs. 0,1%). Ob dies ein Hinweis darauf ist, dass die Impfung auch einen gewissen Schutz vor der Transmission bietet, muss weiter untersucht werden." (AMB 2021).
Eine Studie der amerikanischen CDC an HCWs des Netzwerkes HEROES-RECOVER (Thompson 2021) wird derzeit als weiterer Beweis für die Verminderung auch asymptomatischer Infektionen (und damit des Übertragungsrisikos) durch die Impfung in den Medien zitiert (z.B. tagesschau 29.03.2021) - wohl wegen des (absichtlich?) missverständlichen Satzes "These findings indicate that authorized mRNA COVID-19 vaccines are effective for preventing SARS-CoV-2 infection, regardless of symptom status, among working-age adults in real-world conditions.". Dieser wird in dem Sinne interpretiert, dass die errechnete Impfeffektivität bei asymptomatischen* und symptomatischen Infektionen gleich stark ausgeprägt sei - genau diese Aussage lässt die Studie allerdings nicht zu:
-
untersucht wurden 3950 HCWs von denen im Studienzeitraum 477 einmal, 2479 zweimal geimpft wurden und 994 ungeimpft blieben - verwendet wurden die Impfstoffe von BioNTech und Moderna
-
alle Teilnehmer wurden wöchentlich unabhängig von eventuellen Symptomen und zusätzlich bei Auftreten COVID-19-verdächtiger Symptome einer PCR unterzogen ("routinely tested for SARS-CoV-2 infections every week regardless of symptom status and at the onset of symptoms consistent with COVID-19–associated illness")
-
insgesamt wurden 205 positive PCR-Tests gefunden, von denen 87,3% von COVID-19-typischen, 2% von COVID-19-untypischen und 10,7% von keinerlei Symptomen begleitet wurden
-
aus der Gesamthäufigkeit positiver PCR-Tests und ihrer Verteilung auf Geimpfte und Ungeimpfte werden die bekannten Impfeffektivitäten von etwa 80% nach einer und 90% nach zwei Impfdosen errechnet
-
in den veröffentlichten Studienunterlagen findet sich überhaupt kein Hinweis darauf, wie sich die symptomatischen und die asymptomatischen* Infektionen auf die Geimpften und Ungeimpften verteilen, so dass völlig offen ist, ob und in welchem Umfang die reine Besiedlung durch die Impfungen verringert wird. (Theoretisch könnten ja alle 22 asymptomatischen Fälle bei Geimpften aufgetreten sein - die Studie schweigt sich hierzu aus.) "Regardless of symptom status" bezieht sich also ausschließlich auf die anlasslose Routinetestung, nicht auf die Impfstoffeffektivität. Bei der Effektivität meint "regardless" nur: das haben wir nicht angeschaut...
Eine Studie der kalifornischen Universitäten von San Diego (UCSD) und Los Angeles (UCLA) bei mit mRNA-Impfstoffen geimpften asymptomatischen HCWs fand ein absolutes Risiko positiver PCR-Tests nach Impfung von etwa 1% ("In our cohort, the absolute risk of testing positive for SARS-CoV-2 after vaccination was 1.19% among health care workers at UCSD and 0.97% among those at UCLA") (Keehner 2021). Selbst mehr als 2 Wochen nach der zweiten Impfung wurden noch mit SARS-CoV-2 besiedelte und damit potentiell infektiöse HCWs gefunden:
Eine große Studie des Flughafens in Qatar korrelierte PCR-Abstriche bei ankommenden Reisenden (> 75% Männer) mit vorangegangenen Impfungen (BioNTech oder Moderna, 2. Impfdosis ≥ 14 Tage vor dem Abstrich) oder COVID-19-Erkrankungen. Es zeigte sich, das sowohl die vollständige Impfung, als auch die anamnestische Erkrankung das Risiko eines positiven PCR-Befundes deutlich verminderte:
Die Studie zeigt aber auch, dass selbst nach zweimaliger Impfung ein relevantes Risiko für eine Neubesiedlung besteht und sie hat die deutliche methodische Schwäche, dass die jeweiligen Kontrollgruppen rein anamnestisch definiert sind. Gerade in der Gruppe der untersuchten jungen Männer (medianes Alter 33 Jahre) verlaufen viele SARS-CoV-2-Infektionen a- oder oligosymptomatisch und sind damit als solche nicht erinnerlich - dies verfälscht die Zusammensetzung und damit die Befunde der Kontrollgruppen in unkalkulierbarer Art und Weise (Bertollini 2021).
{slider-1 AZD122 von AstraZeneca}
Eine nachträgliche Analyse von Phase 3-Daten zum Impfstoff von AstraZeneca zeigte bei einem Teil der Studienteilnehmer nach der ersten Impfdosis, dass eine durchgeführte PCR bei Teilnehmern aus der Impfgruppe seltener positiv ausfiel als bei denen der Kontrollgruppe (im Mittel 67% Reduktion bei allerdings geringen absoluten Zahlen) (Voysey 2021). Dies könnte auf eine Verringerung der Übertragungswahrscheinlichkeit auf andere hinweisen und ein Indiz für eine mögliche Herdenimmunität durch den Impfstoff sein. Bei diesen nachgereichten Ergebnissen (untersucht wurde auch die Effektivität nur einer Impfung) weisen allerdings Experten darauf hin, dass beide Punkte keine primären, sondern nachträglich definierte Endpunkte einer für diese Fragestellung nicht konzipierten Studie seien. Damit seien z.B. die Teilnehmer für diese Endpunkte nicht randomisiert - in einem solchen Fall bestünde immer die Gefahr, dass ganz andere, nicht berücksichtigte Faktoren für die beobachteten Effekte verantwortlich seien (so seien z.B. die untersuchten Teilnehmer mit nur einer Impfdosis im Durchschnitt jünger, meist weiblich, meist im Gesundheitswesen tätig und häufiger von weißer Hautfarbe als der Durchschnitt der Teilnehmer (Sample 2021).
Eine weitere, bislang noch nicht wissenschaftlich überprüfte Studie der Universität Oxford zum AstraZeneca-Impfstoff weist in die gleiche Richtung: sie wies nach, dass die Viruslast der Geimpften (gemessen über den ct-Wert der PCR) signifikant geringer war als die der MenACWY-geimpften Kontrollgruppe und die PCR-Positivität im Durchschnitt eine Woche kürzer anhielt (alles Emary 2021) - dies könnte ein Hinweis auf eine verringerte Infektiosität der Geimpften sein (Emary 2021).
Das industrieunabhängige arzneimittel-telegramm hält diese Analyse jedoch für methodisch nicht korrekt und die Ergebnisse für wahrscheinlich überschätzt (a-t 2021)
Der ebenfalls industrieunabhängige Arzneimittelbrief schreibt von einem "geringen Schutz" vor "asymptomatischen Infektionen*" (22%) als Ergebnis der Zwischenanalyse vorliegender Studiendaten (Voysey 2021b) (AMB 2021b)
Die bisher mit Abstand aussagekräftigste Studie zur Frage des Übertragungsrisikos nach Impfung stammt von Public Health England (Harris 2021): hier wurden in mehr als 300.000 Haushalten das Risiko verglichen, sich bei einem infizierten Haushaltsmitglied ("index case") anzustecken, wenn dieses entweder ungeimpft war oder mindestens 21 Tage zuvor entweder Vaxzevria® oder Comirnaty® erhalten hatte. Das Ergebnis ist ernüchternd: "These results show that the likelihood of household transmission is 40-50% lower for households in which the index cases are vaccinated 21 days or more prior to testing positive (compared to no vaccination), with similar effects for both ChAdOx1 nCoV-19 and BNT162b2 vaccines." - das Risiko der Übertragung auf andere wurde nicht einmal halbiert...
(* eine "asymptomatische Infektion" ist streng genommen natürlich keine Infektion, sondern lediglich eine Besiedlung/Kolonisation - auch diese kann jedoch zur Übertragung des Erregers führen; die Begriffe werden in den aktuellen Arbeiten nicht sauber getrennt verwendet)
{/sliders-1}
{slider Literatur}
AMB. 2021, 55, 01. Abruf 28.01.2021
AMB. 2021b, 55, 24
a-t. 2021;51,2
Bertollini R. doi:10.1001/jama.2021.9970
Buss LF. 2021. doi:10.1101/2020.09.16.20194787
CDC. 2020. Vaccines - Glossary. Abruf 28.01.2021
Doshi P. 2020. BMJ 2020;371:m4037.. Abruf 28.01.2021
Emary KRW. Efficacy of ChAdOx1 nCoV-19 (AZD1222) Vaccine Against SARS-CoV-2 VOC 202012/01 (B.1.1.7).
Erlich Y. 2021. doi: https://doi.org/10.1101/2021.02.08.21251329
Fine P. 2011. Vaccines 52; 911-16. Abruf 28.01.2021
Fine P. 1993. Epid Reviews. 15; 265-302.
Hall V. 2021a. http://dx.doi.org/10.2139/ssrn.3790399
Hall V. 2021. https://doi.org/10.1101/2021.01.13.21249642.
Harris RJ. 2021. Impact of vaccination on household transmission of SARS-COV-2 in England
Keehner J. 2021. NEJM. SARS-CoV-2 Infection after Vaccination in Health Care Workers in California. DOI: 10.1056/NEJMc2101927
Levine-Tiefenbrun M. 2021. doi: https://doi.org/10.1101/2021.02.06.21251283
PHE. 2021. Press release 14.01.2021. Abruf 28.01.2021
RKI. 2021. Faktenboxen zur mRNA-Schutzimpfung gegen COVID-19. 26.01.2021
RKI. 2015. Fachwörterbuch Infektionsschutz und Infektionsepidemiologie.
Sample I. 2021. Guardian 02.02.2021. Abruf 05.02.2021
STIKO. 2021. 3. Aktualisierung der COVID-19-Impfempfehlung.
STIKO. 2021b. 4. Aktualisierung der COVID-19-Impfempfehlung.
Sykes W. 2021. DOI: https://doi.org/10.21203/rs.3.rs-233375/v1
tagesschau.de. 29.03.2021. https://www.tagesschau.de/ausland/amerika/mrna-impfstoffe-infektionsrisiko-101.html
Thompson MG. 2021. MMWR April 2, 2021 / 70(13);495–500
Taylor L. 2021. doi: https://doi.org/10.1136/bmj.n394
Voysey M. 2021. https://ssrn.com/abstract=3777268 (preprint)
Voysey M. 2021b. https://doi.org/10.1016/S0140-6736(21)00432-3 (preprint)
Weekes M. 2021. DOI: 10.22541/au.161420511.12987747/v1
{/sliders}