Effektivität
-
Eine schwedische Untersuchung ergab schon sehr früh eine Effektivität der Impfung bezüglich kulturell bestätigten Keuchhustens von lediglich 54 - 64% (Ad hoc group, 1988). Zumindest für Jugendliche und Erwachsene wird diese für eine moderne Impfung schlechte Schutzwirkung in einer Studie aus dem Jahr 2013 fast auf's Prozent genau bestätigt: auch hier betrug die Effektivität 53 - 64% (Baxter 2013).
-
Eine weitere schwedische Studie aus dem Jahr 2012 kommt jedoch zu dem Ergebnis, dass - abweichend von den bisherigen Annahmen - auch im Säuglingsalter eine moderate Schutzwirkung schon durch die erste verabreichte Keuchhustenimpfung erreicht wird (Nilsson 2012), ein Ergebnis, das 2014 von australischen Forschern bestätigt wurde: hier betrug die Schutzwirkung schon der ersten Impfung vor komplizierten Verläufen mit Krankenhausaufenthalt immerhin 55%, weitere Impfungen steigerten diese Effektivität auf knapp 84% (Quinn 2014). Dies wäre insofern interessant, als die kritische Periode für Komplikationen der Erkrankung vor allem die ersten 4, maximal 6 Lebensmonate beträgt.
-
Für Kinder im Alter von 2 bis 7 Jahren schätzt eine Studie aus dem Jahr 2012 die Effektivität auf 41%, zwischen 8 und 12 Jahren sogar nur auf 24% (Misegades 2012).
-
Die Effektivität liegt damit deutlich unter der des "alten" Ganzkeim-Impfstoffs, was sich in einer vergleichenden Studie aus dem Jahr 2013 auch erneut bestätigte (Klein 2013) und schon 2012 in einem Editorial der renommierten Zeitschrift JAMA als "growing consensus", wachsende Übereinstimmung, apostrophiert wurde (Shapiro 2012).
- Beträgt die Schutzwirkung unmittelbar nach der Grundimmunisierung mit dem azellulären Impfstoff (aP) noch etwa 80% (was für eine moderneImpfung wenig ist!), sinkt sie im vierten Jahr nach der Impfung auf etwa 60%, 8 Jahre nach der Impfung auf etwa 40% ab (Schwarz 2016).
-
In den USA, wo die Kinder bis zum 7. Geburtstag 5 Impfdosen Keuchhustenimpfstoff verabreicht bekommen, lässt die Schutzwirkung innerhalb der ersten 5 Jahre nach der 5. Impfdosis pro Jahr um mehr als 40% nach (Klein 2012).
-
In den letzten Jahren kommt es in den meisten Ländern, in denen Keuchhusten (azellulär) geimpft wird, zu einem teilweise dramatischen Wiederanstieg der Erkrankungszahlen - trotz anhaltend hoher oder sogar steigender Durchimpfungsraten. Dies findet seine Erklärung zum einen in der nachlassenden Wirksamkeit des Impfstoffs (s. hierzu diesen Artikel), zum zweiten führt wohl aber gerade der azelluläre Keuchhustenimpfstoff zu einer bisher unterschätzten, großen Zahl keuchhustengeimpfter symptomlos Erkrankender, die dann - weil "Warnsymptome" wie der typische Husten fehlen - unerkannt für Ihre Umgebung ansteckend sind (Althouse 2015). "It is a fact that the currently applied vaccination does not eliminate the circulation of Bordetella pertussis in the community." (Cofré 2015).
-
Von 2000 bis 2012 hat sich in den USA die Zahl der registrierten Keuchhustenfälle versechsfacht - die Autoren einer entsprechenden amerikanischen Studie zitieren das CDC mit der Äußerung "Pertussis continues to be the most poorly controlled bacterial vaccine-preventable disease in this country, despite high rates of DTaP coverage." (CDC 2009, zitiert nach Tartof 2013).
-
Auch langfristig schafft die azelluläre Keuchhustenimpfung Probleme: bei Jugendlichen, die von vorneherein mit Pac grundimmunisiert wurden, liegt die Schutzwirkung vier Jahre nach einer Auffrischung im Schulalter bei unter zehn Prozent!. Die Autoren schlussfolgern: "Routine Tdap did not prevent pertussis outbreaks. Among adolescents who have only received DTaP vaccines in childhood, Tdap provided moderate protection against pertussis during the first year and then waned rapidly so that litle protection remained 2-3 years after vaccination." (Klein 2016)
-
Eine weitere Studie kommt zu dem gleichen Ergebnis: als Auffrischimpfung vermittelt die azelluläre Keuchhustenimpfung einen gewissen Schutz vor allem bei Jugendlichen, die als Kinder initial mit der "alten" Keuchhustenimpfung grundimmunisiert wurden - eine Grundimmunisierung mit der azellulären Impfung scheint keine stabile Immunität zu vermitteln und ein Grund für die Renaissance des Keuchhustens zu sein (Skoff 2016).
-
Als mögliche Lösung dieses Problems wird - neben der mittel- bis langfristigen Entwicklung gänzlich neuer Pertussis-Impfstoffe - auch eine pragmatische Misch-Strategie diskutiert: so würde der Ersatz nur der ersten Keuchhustenimpfung gegen eine "alte" Ganzkeim-Vakzine im Impfschema die Effektivität der Impfstrategie deutlich erhöhen - allerdings müsste man nach Ansicht der Autoren einer diesbezüglichen Arbeit natürlich den deutlichen Anstieg der Impfnebenwirkungen dagegen halten... (DeAngelis 2016).
-
Zusammenfassend spricht angesichts dieser Datenlage auch das RKI davon, dass, obwohl die klassischen Keuchhustenerreger nur beim Menschen vorkommen, “aus heutiger Sicht ... eine Eradikation von Pertussis im Gegensatz zu anderen impfpräventablen Krankheiten nicht möglich" ist (RKI 2010).
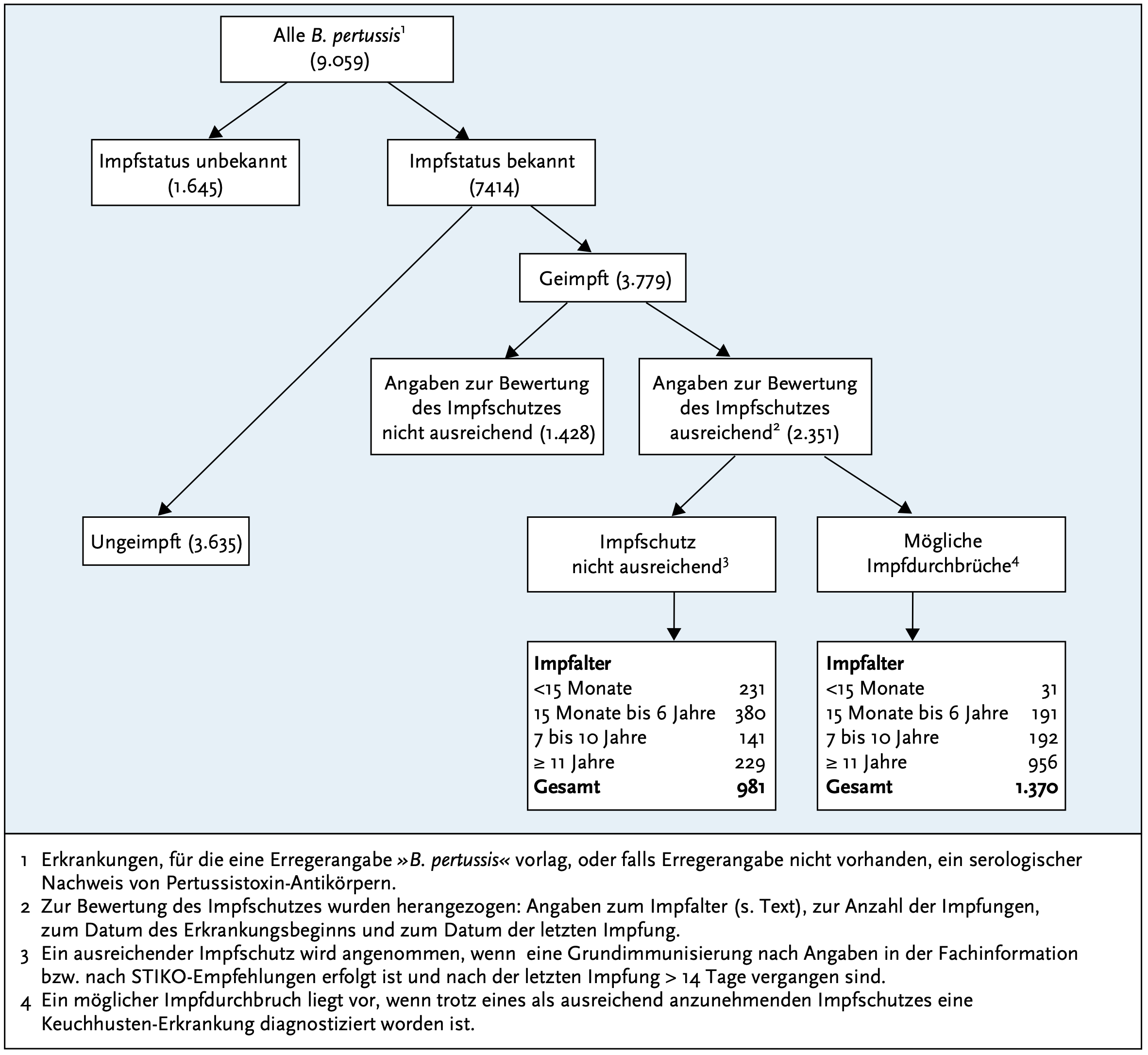
- Auch die Auswertung der Meldezahlen von Keuchhustenerkrankungen in D bestätigen die insgesamt unbefriedigende Wirkung der Impfung - so waren 2019 von 5986 Erkrankten mit auswertbarem Impfstatus ((3.635 Erkrankte mit der Angabe, nie geimpft worden zu sein, und 2.351 Erkrankte mit vollständigen Angaben zu erhaltenen Impfungen) 1370 (mithin 23%) altersentsprechend geimpft, also klassische Impfversager
(Quelle RKI 2020)
-
Zusätzlich beunruhigend sind Ergebnisse aus tierexperimentellen Studien, die nahelegen, dass speziell der azelluläre Keuchhusten-Impfstoff zwar einen (mäßigen) Schutz vor dem "klassischen" Keuchhusten (ausgelöst durch Bordetella pertussis) vermittelt, dafür aber die Anfälligkeit für Infektionen mit B. parapertussis deutlich erhöhen könnte (Long 2010).
-
Auch wenn Erkrankungen durch B. parapertussis in der internationalen Literatur als weniger schwer eingeschätzt werden, sieht das RKI dies nicht ganz widerspruchsfrei anders - auf der einen Seite geht es in Übereinstimmung mit der Mehrzahl aktueller Studien davon aus: " Der verwandte Erreger B. parapertussis hat kein Pertussis-Toxin-Gen und verursacht daher ein zwar ähnliches, aber milderes klinisches Bild" (RKI 2009) - auf der anderen Seite dramatisiert es im Rahmen der Meldeverpflichtung auch für B. parapertussis-Fälle "In der neuen Version [der Keuchhusten-Übersichtsveröffentlichung des RKI], die in Kürze erscheinen wird, stellen wir klar, dass auch Personen, bei denen B. parapertussis als Ursache für einen Keuchhusten nachgewiesen wird vom Besuch von Gemeinschaftseinrichtungen ausgeschlossen werden müssen. Die Begründung liegt in der hohen Kontagiosität und der Gefahr insb. für Säuglinge, die auch an einer Keuchhusten-Erkrankung durch B. parapertussis schwer erkranken können" (RKI 2017 - pers. Mitteilung)
"Kokon-Strategie"
-
Da die jungen Säuglinge im überhaupt durch Komplikationen gefährdeten Alter der ersten 4 - 6 Lebensmonate durch die aktuellen Impfstrategien und den schlecht wirksamen Impfstoff nicht befriedigend geschützt werden können, hat die STIKO vor einigen Jahren - wie andere nationale Impfkomissionen auch - die flächendeckende Impfung aller Erwachsenen empfohlen: sie sollen den Säugling in einen schützenden Kokon (aus Geimpften) hüllen.
-
Wie dies jedoch gelingen soll, wo die Impfung (s.o.) keine überzeugende Schutzwirkung vor der Erkrankung und noch viel weniger vor der Übertragung bietet, bleibt jedoch offen.
-
Eine kanadische Untersuchung aus dem Jahr 2014 unternahm den Versuch zu berechnen, wie viele Erwachsene denn geimpft werden müssten (NNV - number needed to vaccinate), um jeweils einen Erkrankungsfall, einen Fall von im Krankenhaus behandlungspflichtig kompliziertem Verlauf von Keuchhusten und einem Todesfall zu verhindern. Für das Verhindern eines einzigen Erkrankungsfalles müssten dieser Studie nach zwischen 500 und 60.000 Menschen, für das Verhindern eines keuchhustenbedingten Krankenhausaufenthaltes 12.000 bis 300.000 und für das Verhindern eines keuchhustenbedingten Todesfalles 1 Million bis mehr als 30 Millionen Menschen geimpft werden. Auch wenn die berechnungsbedingt extrem große Spannbreite der jeweils notwendigen Impfzahlen (die sich z.B. aus der nicht berechenbaren Annahme von nicht gemeldeten Keuchhustenfällen (underreporting) ergibt) jede konkrete Berechnung verbietet, so zeigt sich doch, dass hier wohl in keinem Fall ein vernünftiges Verhältnis zwischen Aufwand (und Risiko der Geimpften!) und entstehender Schutzwirkung erwartet werden kann (Lim 2014).
-
Eine niederländische Studie von 2014 identifizierte vollständig (keuchhusten-) geimpfte Geschwisterkinder als die wichtigste Ansteckungsquelle für Säuglinge in den ersten 6 Lebensmonaten (Bertilone 2014) - diese Ergebnisse führen die Kokonstrategie, die die Pertussisimpfung von Gschwisterkindern ja gerade empfiehlt, um die Ansteckung zu vermeiden, komplett ad absurdum.
-
Eine Studie aus dem Jahr 2015 geht noch einen Schritt weiter spricht von einem "mehrfach nachgewiesenen Versagen" der Kokonstrategie (Healy 2015, Castagnini 2012) und erklärt dies mit der Zunahme keuchhustengeimpfter, symptomloser Keuchhustenkranker unter der aktuellen Impfstrategie mit dem azellulären Impfstoff (Althouse 2015). Auch die WHO betont ausdrücklich, dass sie die Kokonstrategie nicht empfiehlt: "Neo-natal immunization, and vaccination of pregnant women and household contacts (“cocooning”) against pertussis is not recommended by WHO. " (WHO 2015)
-
Und das amerikanische Center for Disease Control fasst zusammen: "Since pertussis spreads so easily, vaccine protection decreases over time, and acellular pertussis vaccines may not prevent colonization (carrying the bacteria in your body without getting sick) or spread of the bacteria, we can't rely on herd immunity to protect people from pertussis." (CDC 2015)
-
Fachleute diskutieren daher seit längerem ernsthaft eine Abkehr vom derzeitigen Impfstoff mit einer vorübergehenden Rückkehr zu "alten" Keuchhustenimpfung und betonen die Notwendigkeit, einen völlig neuen Impfstoff zu entwickeln (Carbonetti 2015).
Nebenwirkungen
- Grund für die Einführung des „neuen“, azellulären Impfstoffes war vor allem die Erwartung der Reduktion der für den „alten“ Impfstoff charakteristischen schweren Nebenwirkungen.
- In Japan, wo die azelluläre Keuchhustenimpfung zuerst in größerem Maßstab durchgeführt wurde, ergaben erste Untersuchungen, dass die Rate der milden UAW (Fieber, Unruhe etc.) um ca. 60% sank, die der sehr seltenen schweren UAW blieb in etwa gleich verglichen mit dem „alten Keuchhustenimpfstoff“ (Noble 1987).
- In Schweden gab es ähnliche Ergebnisse: es kam zu 2 schweren enzephalopathische Erkrankungen (bei 212 Impfdosen, 1 : 100) (Ad hoc group 1988), daher wurde der Impfstoff 1989 nicht zugelassen.
- Beschrieben wurde mittlerweile auch die Manifestation einer schweren, fortschreitenden Hirnschädigung (Rett-Syndrom-artige Enzephalopathie) wenige Stunden nach der aP-Impfung (Fiumara 2002)
-
Die Häufigkeit von Krampfanfällen insgesamt innerhalb von 3 Tagen nach der Impfung wurde für den „alten Impfstoff“ (DPT) auf 1 : 4000, für den „neuen Impfstoff“ (DPacT) immerhin noch auf 1 : 16000 berechnet (Uberall 1997).
-
Speziell beim azellulären Keuchhustenimpfstoff scheint der frühe Impfbeginn wie in Deutschland empfohlen problematisch zu sein: systemische Nebenwirkungen sind bei der Impfung im Alter von 2 Monaten signifikant häufiger, als bei späterer Impfung (Korkmaz 2013) - diese deutliche Altersabhängigkeit fand sich beim "alten" Keuchhustenimpfstoff in dieser Untersuchung nicht (obwohl dieser insgesamt deutlich mehr Nebenwirkungen hervorrief...).
-
Schockartige Zustände mit Verlust des Muskeltonus und fehlender Ansprechbarkeit der Kinder (Hypoton-Hyporesponsive Episoden HHE, s. o.) wurden auch nach Anwendung des azellulären Impfstoffes beobachtet (Goodwin 1999, Heininger 1999, DuVernoy 2000).
-
Auch bei Erwachsenen, die aktuellen Impfempfehlungen zu Folge auch (in Österreich sogar regelmäßig) gegen Keuchhusten geimpft werden sollen, lässt die Verträglichkeit der Impfung deutlich zu wünschen übrig: eine Studie aus dem Jahr 2012 weist hier schwere neurologische (Guillain-Barré-Syndrom, Demyelinisierende Erkrankungen) und allergische UAWs nach (Chang 2012).
-
Es gibt zunehmend Hinweise darauf, dass eine Keuchhusteninfektion nach vorangegangener (azellulärer) Impfung eine besonders riskante Situation darstellt, da es hierbei (anders als bei nicht geimpften Kindern) zu einer deutlich allergieassoziierten Immunantwort kommt (Hendrikx 2011) - dies unterstützt die klinische Beobachtung, dass für diese Kinder ein deutlich erhöhtes Asthma-Risiko besteht.
Literatur:
Ad hoc group for the study of pertussis vaccine. Lancet 1988; 1:955-960.
Althouse BM. BMC Medicin (2015) 13:146. Abruf 25.06.2015
Baxter R. BMJ 2013;347:f4249. Abruf 15.11.2013
Bertilone C. Commun Dis Intell Q Rep. 2014 Sep 30;38(3):E195-200. Abruf 25.06.2015
Carbonetti N. FEMS Pathogens and Disease, 73, 2015, ftv090 (Abruf 11.02. 2016)
Castagnini LA.Clin Infect Dis. 2012 Jan 1;54(1):78-84. doi: 10.1093/cid/cir765. Abruf 25.06.2015
CDC. MMWR Morb Mortal Wkly Rep. 2011;58(53):1–100
CDC 2015: Pertussis FAQs. Abruf 01.08.2016
Chang S. Vaccine 2012 Nov 8. pii: S0264-410X(12)01570-8. doi: 10.1016/j.vaccine.2012.10.097.
Cofré J. Rev. chil. infectol. vol.32 no.5 Santiago Oct. 2015. Abruf 05.07.2016
DeAngelis H. JAMA Pediatr. 2016 Mar 28. doi: 10.1001/jamapediatrics.2016.0047. (Abruf 30.03.2016)
Duvernoy TS. Pediatrics 2000 Oct;106(4):E52
Fiumara A. J Child Neurol. 2002 Sep;17(9):700-2.
Goodwin HJ. Paediatr. Child Health 1999 Dec;35(6):549-52
Healy CM. Pediatr Infect Dis J. 2015 Jan;34(1):22-6. Abruf 25.06.2015
Heininger U. Cons Infect 1999
Hendrikx LH. Vaccine. 2011 Sep 16;29(40):6874-80.
Klein N. Kaiser Permanente Press Release vom 05.02.2016 (Abruf 11.02.2016)
Klein NP. N Engl J Med 2012; 367:1012-1019 September 13, 2012DOI: 10.1056/NEJMoa1200850
Klein NP. Pediatrics Vol. 131 No. 6 June 1, 2013. pp. e1716 -e1722. (doi: 10.1542/peds.2012-3836)
Korkmaz HA. Paediatr Int Child Health. 2013 Dec 19.
Lim GH. Euro Surveill. 2014;19(5):pii=20688.
Long GH. 2010. Proceedings of the Royal Society B: Biological Sciences. 277(1690):2017–25
Misegades LK. Clin Infect Dis. (2012) 55 (10): 1432-1433. doi: 10.1093/cid/cis669
Nilsson L. Vaccine. 2012 May 2;30(21):3239-47.
Noble GR. JAMA 1987; 257:1351-1356.
Quinn HE. PEDIATRICS Volume 133, Number 3, March 2014.
RKI. 2009. Epid Bull 31/2009
RKI. Pertussis - Stand 2010. Abruf 15.11.2013
Schwarz KL. CMAJ. 2016 Nov 1;188(16):E399-E406. Abruf 10.04.2017
Shapiro ED. JAMA 2012 Nov 28; 308 (20):2149-50
Skoff TH. JAMA Pediatr. 2016 May 1;170(5):453-8. doi: 10.1001/jamapediatrics.2015.4875. Abruf 07.07.2016
Tartof SY. PEDIATRICS Volume 131, Number 4, April 2013 (Abruf 11.02.2016)
Uberall MA. Dev Biol Stand1997; 89:83-9
WHO. Recommendations for routine immunization. (Abruf 20.02.2016)