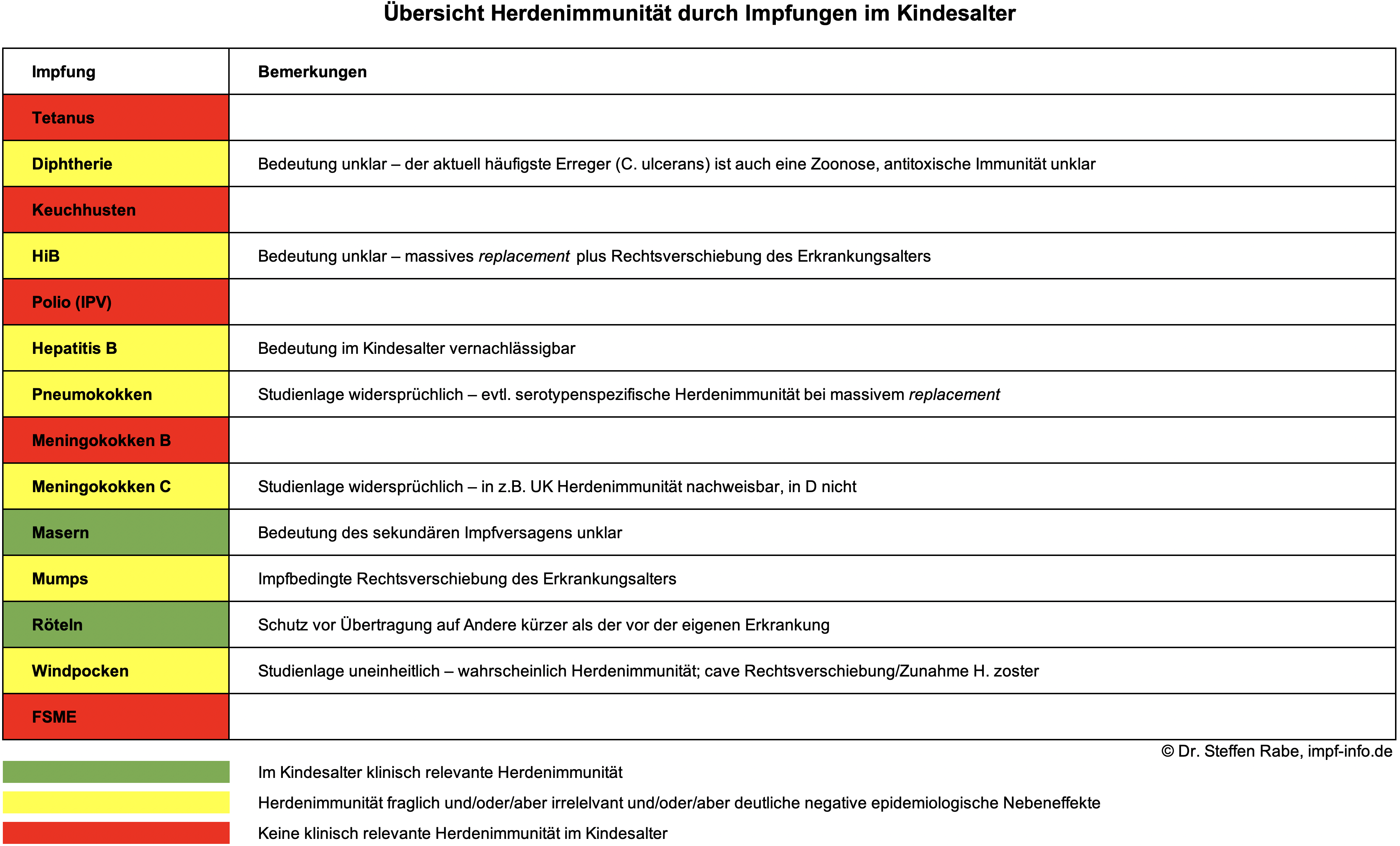
Das Argument der so genannten Herdenimmunität scheint in der aktuellen Impfdiskussion das Universalargument zum Beenden jeder impfkritischen Diskussion zu sein: Impfen, um andere zu schützen, die sich in Einzelfällen nicht selber schützen können. Was ist eigentlich Herdenimmunität?
Die Geschichte des Begriffs der "Herdenimmunität", die im humanmedizinischen Bereich im Anfang des 20. Jahrhunderts beginnt, ist von Anfang an eine Geschichte von Missverständnissen und willkürlichen (Teil-)Definitionen, wie Fine in zwei wesentlichen Arbeiten 1993 und 2011 feststellt:
"The term ‘‘herd immunity’’ is widely used but carries a variety of meanings […]. Some authors use it to describe the proportion immune among individuals in a population. Others use it with reference to a particular threshold proportion of immune individuals that should lead to a decline in incidence of infection. Still others use it to refer to a pattern of immunity that should protect a population from invasion of a new infection. A common implication of the term is that the risk of infection among susceptible individuals in a population is reduced by the presence and proximity of immune individuals (this is sometimes referred to as ‘‘indirect protection’’ or a ‘‘herd effect’’)" [Der Begriff der "Herdenimmunität" ist weit verbreitet und trägt eine Vielzahl von Bedeutungen [Literaturzitate in der Originalarbeit]. Einige Autoren nutzen ihn, um den Anteil Immuner in einer Bevölkerung zu beschreiben. Andere verwenden ihn mit Bezug auf einen definierten Anteil immuner Individuen, der zu einer Abnahme der Inzidenz einer Infektion führen solle. Wieder andere nutzen ihn hinsichtlich eines Immunitätsmusters, das eine Bevölkerung vor dem Ausbrechen einer neuen Infektionskrankheit schützen solle. Eine übliche Bedeutung des Begriffs ist, dass das Risiko der Infektion für empfängliche Individuen in einer Bevölkerung durch das Vorhandensein immuner Individuen verringert wird (dies wird manchmal auch als "indirekter Schutz" oder "Herdeneffekt" bezeichnet.] (Fine 2011).
Von wirklicher epidemiologischer Relevanz sind zwei (Teil-)Aspekte der Herdenimmunität:
-
zum einen, dass in einer Bevölkerung so viele Menschen immun sind, dass jemand, der für diese Erkrankung ansteckend ist, auf so wenige Nicht-Immune trifft, dass er im Durchschnitt weniger als eine weitere Person ansteckt (die effektive Reproduktionszahl R wäre damit kleiner als 1 und eine Epi/Pandemie käme zum Erliegen (s. hier). Für diesen Aspekt der Herdenimmunität ist eine "sterile Immunität", die die Weitergabe der Erkrankung durch Immune verhindert, nicht zwingend erforderlich.
-
zum anderen, dass Nicht-Immune in einer Bevölkerung dadurch geschützt werden, dass sie im Wesentlichen von Immunen umgeben sind, die aufgrund der eigenen Immunität die Erkrankung auch nicht mehr weitergeben. Unabdingbare Voraussetzung für dieses Verständnis der Herdenimmunität ist natürlich, dass die Immunität des/der Einzelnen nicht nur vor der eigenen Erkrankung schützt, sondern auch vor der Weitergabe des Krankheitserregers an andere ("sterile Immunität").
Dieser letzten Bedeutung - den Schutz grundsätzlich Empfänglicher vor Ansteckung durch die Immunität der anderen - schließen sich heute die Mehrzahl der fachkundigen Autoren und auch die Gesundheitsbehörden an (Hervorhebung von mir):
-
"Herdenschutz (engl.: heard immunity) Herdenimmunität; der Effekt, dass ein gewisser Anteil immuner Individuen innerhalb einer Population (entstanden durch Impfung oder abgelaufene Infektionen) auch nichtimmunen Personen einen relativen Schutz bietet" (RKI 2015 - Rechtschreibfehler heard (eigentlich: herd) im Original)
- Community immunity: A situation in which a sufficient proportion of a population is immune to an infectious disease (through vaccination and/or prior illness) to make its spread from person to person unlikely. Even individuals not vaccinated (such as newborns and those with chronic illnesses) are offered some protection because the disease has little opportunity to spread within the community. Also known as herd immunity. (CDC 2020).
-
Jede Infektionskrankheit hat eine charakteristische so genannte Basisreproduktionszahl R0
-
Diese ist ein Maß für die Infektiosität der Erkrankung - wieviele Ungeschützte steckt ein Kranker in einer Bevölkerung, in der keinerlei Immunität gegen diese Erkrankung besteht, an? Kurz gefasst: je höher diese Zahl, desto ansteckender die Erkrankung.
-
R0 muss für die Ausbreitung einer Erkrankung immer größer als 1 sein, sonst käme die Krankheit von alleine zum Erliegen
-
Aus dieser "Basisreproduktionszahl" ist die Herdenimmunitätsschwelle (H) errechenbar – wieviele Menschen müssen gegen eine Erkrankung immun sein, damit eine Herdenimmunität auftritt, die auch an sich Ungeschützte vor der Ansteckung schützt? Es gilt:
-
H = 1 - 1/R0 (Fine 1993)
-
-
Beispiele für diese Werte sind (Smith 2010, Fine 1993)
-
Für realistische Betrachtungen ist es wichtig zu bedenken, dass die tatsächliche Infektiosität immer geringer ist, weil in jeder Bevölkerung ein kleinerer oder größerer Anteil gegen jede Erkrankung bereits immun ist (I) -
-
sei es durch eine durchgemachte Erkrankung, also eine natürlich erworbene Immunität (IN),
-
sei es durch eine Impfung (IV).
-
I ist demnach die Summe aus IN und Iv, es gilt also I = IN + IV
-
-
Dieser Anteil muss beim Berechnen der Reproduktionszahl berücksichtigt werden und ergibt dann die effektive Reproduktionszahl R, die regelmäßig kleiner ist als R0
-
R = R0 (1 - I)
-
-
Wichtig ist hier, dass weder die Herdenimmunitätsschwelle (H), noch die impfbedingten Immunität (Iv) mit der notwendigen Durchimpfungsrate VC gleichzusetzen ist - beide H und Iv meinen ja den Anteil der tatsächlich immunen Menschen in einer Bevölkerung.
-
Keine Impfung schützt 100% aller Geimpften, so dass die Zahl der durch die Impfung Immunen regelmäßig kleiner ist als die Zahl der Geimpften - dies wird ausgedrückt durch die Angabe der Impfeffektivität E - sie gibt an, um wieviel geringer das Risiko zu erkranken bei Geimpften im Vergleich zu einer ungeimpften Vergleichsgruppe ist. Erst mit ihrer Kenntnis kann aus der Zahl der Geimpften die Zahl der durch Impfung tatsächlich Geschützten (Iv) errechnet werden.
-
Will man also die für das Entstehen einer durch die Impfung bedingten Herdenimmunität nötige kritische Durchimpfungsrate VC errechnen, müssen H und E bekannt sein und berücksichtigt werden:
-
VC = H / E
-
-
Auch diese Formel geht von einer Bevölkerung aus, in der sich Infizierte und Geimpfte gleichmäßig verteilen und in der keine natürliche Immunität (In), sondern nur die Impf-Immunität (Iv) besteht.
-
Möchte man diese - bei allen impfrelevanten Erkrankungen in Europa vorhandenen - Anteil natürlich Immuner berücksichtigen, wird die Formel noch etwas komplexer (Plans-Rubió 2012):
-
VC = (H - IN) / E = [(1 - (1/R0)) - IN] / E
-
-
Gleichzeitig zeigt diese Formel eindrücklich, dass wenn die Impfstoffeffektivität E kleiner ist als die Herdenimmunitätsschwelle H, eine Eliminition einer Erkrankung selbst bei vollständiger Durchimpfung unmöglich ist (dann ergäbe nämlich H / E einen Wert > 1 - es müssten also mehr als 100% der Bevölkerung geimpft werden...)
-
Da Tetanus nicht von Mensch zu Mensch übertragen wird, sondern die Infektion durch entsprechende Verletzungen stattfindet, kann Herdenimmunität hier keine Rolle spielen.
-
Das verhindert aber nicht, dass die Impfpflicht für Wundstarrkrampf dennoch regelmäßig politisch gefordert wird (z.B. auf dem Bundesparteitag der CDU 2015 (CDU 2015)).
-
Und es kann auch nicht die Herdenimmunität dafür verantwortlich sein, dass die Erkrankung insgesamt sehr selten auftritt - obwohl in Deutschland mehr als 500.000 Kinder nicht gegen Wundstarrkrampf geimpft sind (RKI 2016), trat seit mehr als 25 Jahren kein Todesfall bei Kindern auf, der durch Impfungen hätte verhindert werden können (GBE 2016).
-
wie unvorhersehbar Herdenimmunitätseffekte sich im Einzelfall einstellen (oder eben auch nicht - s. Keuchhustenimpfung), lässt sich auch an der Diphtherie-Impfung sehen: hier vermittelt die Impfung eigentlich ausschließlich einen Schutz vor der Giftwirkung derjenigen Diphtheriebakterien (DB - so genannte antitoxische Immunität), die dieses Gift bilden, also "toxigen" sind. Weder die Infektion mit den Bakterien, noch deren Weitergabe an Andere wird von der Impfung unmittelbar beeinflusst (RKI 2009), eine "klassische" Herdenimmunität kann daher nicht entstehen.
-
Studien, die eine große Impfkampagne (> 30 Millionen Impfdosen) in Rumänien Ende der 1950er Jahre begleiteten, zeigten jedoch, dass etwas zeitversetzt zur Massenimpfung der Anteil der toxigenen DB an den DB überhaupt und Rumänien von über 90% vor der Kampagne auf unter 5% nach der Kampagne sanken - ein "unforeseen result of mass vaccination" (Pappenheimer 1984, Saragea 1979). Eine Erklärung für diesen völlig unerwarteten Impf-Effekt sucht man darin, dass in einer geimpften Bevölkerung toxigene Diphtheriebakterien ihren evolutionsbiologischen Vorteil einbüßen und daher gegenüber nicht-toxigenen DB in der Häufigkeit abnehmen - bei gleichbleibender Gesamthäufigkeit von DB in Rachenabstrichen der Bevölkerung.
-
Hier wäre eine angenommene Herdenimmunität also auf bakteriell-evolutionsbiologischer Ebene angesiedelt, hinterlässt aber eine Reihe von Fragen:
-
die 60 Jahre alten rumänischen Untersuchungen wurden so nie wiederholt und die Ergebnisse damit nie reproduziert
-
in allen westlichen Ländern ist die Diphtherie-Immunität im Erwachsenenalter völlig unzureichend, meist sind - wie in Deutschland (RKI 2009) - weit weniger als die Hälfte der Erwachsenen noch immun. Dennoch bleibt ein Wiederauftreten der Diphtherie-Epidemien vergangener Jahrzehnte aus. Ein möglicher Erklärungsansatz wäre hier, dass die mit dem Einführen von Massenimpfkampagnen oft parallel gehende deutliche Verbesserung der sozioökonomischen Situation der Bevölkerung an der epidemiologischen Stabilität einen nennenswerten Anteil hat (Glatman-Freedman 2012).
-
-
Wichtig ist, dass der Einzelne trotz vorhandenen Impfschutzes sehr wohl andere Menschen mit Diphtherie infizieren kann - die Herdenimmunität funktioniert hier tatsächlich nur "im großen (nämlich bevölkerungsweiten) Maßstab" (Edwards 2018) - "Da sich die Diphtherie-Impfung gegen das Diphtherietoxin richtet und nicht gegen den Diphtherie-Erreger, kann es auch bei Geimpften zu einer Besiedelung mit toxigenen Erregern kommen, ohne dass Toxin-bedingte Symptome vorliegen." (RKI 2020)
-
Ein weiteres Problem bei der Diphtherie ist das in allen westlichen Ländern zu beobachtende, zunehmende Auftreten von Corynebacterium ulcerans.
-
Dieser Erreger ist auch in Deutschland in den letzten 15 Jahren häufiger als das „klassische“ Diphtheriebakterium Corynebacterium diphtheriae (s. hier) als Erreger einer Diphtherie nachzuweisen und birgt 2 gravierende Probleme:
-
Erstens ist nicht klar, ob der aktuelle Impfstoff auch gegen das Toxin von C. ulcerans wirkt [28] (was ggf. langfristig auch die Herdenimmunität kompromittierte) - das RKI hält bei den drei 2019 aufgetretenen Fällen von Diphtherie trotz bestehenden Impfschutzes ("Impfversagen") eine verminderte Wirksamkeit der Impfung gegen C. ulcerans ausdrücklich für eine mögliche Erklärung (RKI 2020).
-
zweitens sind – im Gegensatz zu C. diphtheriae – bei C. ulcerans auch Haustiere ein klinisch relevantes Erregerreservoir (RKI 2011), was eine Herdenimmunität bei Menschen in ihrer Bedeutung für die Ausbreitung der Erkrankung stark einschränkt.
-
-
Auch bei der Keuchhustenimpfung vermittelt die Impfung einen (mäßigen und nur relativ kurzen) Schutz vor der Erkrankung.
-
Die "moderne", so genannte azelluläre Keuchhustenimpfung schützt aber offenbar kaum vor Besiedlung mit dem Keuchhustenbakterium oder vor dessen Weiterverbreitung an andere - das heißt Geimpfte können sich anstecken und wiederum andere anstecken, ohne (typisch) zu erkranken.
-
"Finally, aPV pertussis vaccines do not prevent colonization. Consequently, they do not reduce the circulation of B. pertussis and do not exert any herd immunity effect. These findings at least partly explain the resurgence of pertussis." (Esposito 2019 [Hervorhebung von mir]; auch Althouse 2015, Warfel 2014).
-
Die amerikanische Gesundheitsbehörde CDC fasst dies so zusammen [Hervorhebung von mir]
-
„Since pertussis spreads so easily, vaccine protection decreases over time, and acellular pertussis vaccines may not prevent colonization (carrying the bacteria in your body without getting sick) or spread of the bacteria, we can't rely on herdimmunity to protect people from pertussis.“ (CDC 2015)
-
-
Auch die amerikanische Behörde für Arzneimittelsicherheit FDA geht nicht von einer Herdenimmunität bei Keuchhusten aus:
-
"[…] although people immunized with acellular vaccines may be protected […] they may still become infected. And these people can then infect others, including infants." (FDA 2016)
-
-
Dies stellt die in Deutschland massiv propagierte "Kokon-Strategie" (die Impfung von Eltern, Großeltern, Geschwistern etc., um z.B. einen Säugling zu schützen) in Frage. Zu dieser schreibt eine immunologische Arbeit aus dem Jahr 2023 lapidar: "For the cocooning strategy to be effective, the aP vaccine would have to generate sterilizing herd immunity, preventing Bp colonization in close contacts of vulnerable infants. This is not possible with the current aP vaccine." (Callender 2023).
-
Die nicht als impfkritisch bekannte WHO empfiehlt demnach die Kokon-Strategie bei Keuchhusten ausdrücklich nicht [Hervorhebung von mir].
-
„Neonatal immunization, and vaccination of pregnant women and household contacts (“cocooning”) against pertussis is not recommended by WHO“ (WHO 2016)
-
-
Der letzte in Deutschland erworbene Fall von Kinderlähmung trat 1990, der letzte importierte Fall 1992 auf.
-
Obwohl in Deutschland allein mehr als 600.000 Kinder und Jugendliche unter 18 Jahren nicht gegen Polio geimpft sind (RKI 2016), kam es seitdem zu keinen weiteren Fällen.
-
Auch dies ist durch eine Herdenimmunität nicht erklärbar, denn in Deutschland wird seit langem nur noch die so genannte IPV-Impfung durchgeführt (gespritze Impfung mit abgetöteten Polio-Viren im Gegensatz zur früher durchgeführten OPV, der Schluckimpfung), und für die IPV gilt:
-
„Die IPV-Impfung [...] schützt die Geimpften zuverlässig vor Erkrankung […].
-
Mit IPV geimpfte Personen können sich aber dennoch mit Polio-Viren infizieren und diese unbemerkt ausscheiden und dadurch weiterverbreiten.“ (RKI 2015)
-
Die IPV scheint begrenzt die Weitergabe der Polioviren über den Nasen-Rachen-Raum zu verringern, ein Übertragungsweg, der gerade in Ländern mit guten sanitären Verhältnissen (die die typische Polio-Infektion über mit Fäkalien verschmutztes Trinkwasser verhindern) eine relevante Rolle spielt (Fox 1980).
-
-
Es tritt also erstens bei der IPV nicht nur keine sichere Herdenimmunität auf (RKI 2015) - diese vermittelt nur die Schluckimpfung (OPV), die aber, weil sie das Risiko einer Kinderlähmung durch die Impfung selber in sich birgt, in Deutschland seit 1998 nicht mehr empfohlen ist.
- Sondern, zweitens, im Gegenteil - die IPV erhöht sogar potentiell die Zahl derer, die (weil selber geschützt) bei einer Infektion mit Polioviren nicht erkranken, die Viren aber dennoch übertragen können (s. hier) - dies ist das Gegenteil einer Herdenimmunität...
-
Masern sind eine hochansteckende Erkrankung (Kontagions- und Manifestationsindex nahe 100%, d.h. bei Kontakt stecken sich fast alle Nicht-Immunen an und erkranken auch typisch (RKI 2014)).
-
"an asymptomatic carrier state has not been documented" (CDC 2015).
-
Nach einer ersten Masernimpfung im zweiten Lebensjahr sind etwa 95% der Geimpften ausreichend geschützt, unabhängig von einer zweiten Impfung (Strebel 2017).
-
Lässt die Schutzwirkung der Masernimpfung dann nach (so genanntes sekundäres Impfversagen), kommt es bei erneutem Viruskontakt zu so genannten vaccine modified-measles mit oft untypischem Krankheitsbild.
-
Auch diese Form von Masern ist grundsätzlich ansteckend, wenn auch das Ausmaß der Infektiosität derzeit noch unklar ist (s. dazu hier) - von dieser Infektiosität wird aber die Zukunft der Masern-Epidemiologie entscheidend abhängen.
-
Grundsätzlich vermittelt die Masernimpfung eine Herdenimmunität, d. h. der (noch) wirksam Geimpfte kann Nicht-Immune nicht anstecken.
-
In einer Analyse US-amerikanischer Masernfälle von 2001 - 2017, konnte dies erstmals auch quantitativ untersucht werden (Gastañaduy 2019): es zeigte sich,
-
erstens, dass R (also die effektive Reproduktionszahl) in einem Land mit hoher Durchimpfungsrate wie den USA mit einem Wert von 0,76 deutlich unter R0 für Masern liegt - echte Epidemien sind bei R < 1 nicht mehr zu erwarten.
-
zweitens, dass eine einmalige Masernimpfung diesen Wert deutlich vermindert auf R = 0,17
-
drittens, dass eine zweimalige Masernimpfung diese Verminderung keineswegs verbessert - der Wert für zweimal Geimpfte lag bei R = 0,27; ein klares Indiz dafür, dass die zweite Masernimpfung auch unter epidemiologischen Aspekten maßlos überschätzt wird.
-
-
Welche Rolle in diesem Zusammenhang die vaccine modified-measles zukünftig spielen werden, ist derzeit völlig unklar.
-
Hier könnte der nachlassende Schutz ein großes Problem darstellen, da aus Titeruntersuchungen bekannt ist, dass für den Schutz vor einer Masernübertragung auf andere wesentliche höhere Antikörperspiegel erforderlich sind, als für den Schutz vor der Erkrankung selber (s. hier - Plotkin 2010).
-
Angesichts der relativ niedrigen Basisreproduktionszahl (s.o.) und der in vielen Länder hohen Durchimpfungsraten müsste dort rein mathematisch längst eine stabile Herdenimmunität, ja, sogar eine Elimination der Mumps erreicht sein (Anderson 1987).
-
Diese mathematischen Modelle tragen offensichtlich unter Bedingungen der wirklichen Welt nicht, was auch daran liegt, dass die Mumpsimpfung - anders als z.B. die Masernimpfung - nicht zuverlässig vor der Übertragung von Wildviren an Andere schützt (ähnlich wie beim Keuchhusten) (Fanoy 2011, Rota 2009, Cortese 2008). Serologische Studien lassen annehmen, dass auf jeden erkrankten Geimpften statistisch drei ebenfalls ansteckende, aber nicht klinisch erkrankte Geimpfte kommen (Dittrich 2011) „Consequently, in an outbreak setting, the role of asymptomatic infections to disease spread may be substantial.“ (Rubin 2017). Demgegenüber geht eine Analyse der ehemals renommierte Cochrane (-Collaboration) von einer Impfstoff-Effektivität bezüglich der Übertragung auf z.B. Haushaltskontaktpersonen vn 74% aus, bei mäßiger Zuverlässigkeit der Evidenz (Di Pietrantonj 2021).
-
Die Mumps-Impfung schützt nicht nur den einzelnen Geimpften ausgesprochen schlecht vor der Erkrankung (bei größeren amerikanischen oder europäischen Epidemien der letzten Jahre waren jeweils 75 - 89% der Erkrankten mindestens zweimal, teilweise dreimal Mumps geimpft (CDC 2016, CDC 2010, Dayan 2008), sie hat die tatsächliche Herdenimmunität in der Bevölkerung darüber hinaus auch noch substantiell verschlechter:
-
vor der Einführung der flächendeckenden Mumpsimpfung hatten 90% der amerikanischen Kinder Mumps bis zum 14. Geburtstag durchlebt (Quinlisk 2010)
-
seit der Einführung der flächendeckenden Mumpsimpfung liegt das Haupterkrankungsalter bei Mumps zwischen 15 und 19 Jahren (RKI 2013)
-
das ist bedeutsam, weil die gefürchtete Hodenentzündung mit der Gefahr der Unfruchtbarkeit bei Mumpserkrankungen im Kindesalter (fast) unbekannt ist, ab der Pubertät die Hodenentzündung aber bei bis zu 30% der betroffenen Männer auftritt.
-
mit anderen Worten waren ohne Mumpsimpfung 90% der Bevölkerung im kritischen Alter vor einer der kritischsten Komplikationen der Mumps (lebenslang und zuverlässig) geschützt - weil sie die Erkrankung bereits hinter sich hatten und immun waren.
- einen solchen Schutz kann die Impfung nach heutigem Kenntnisstand nicht gewährleisten.
-
-
Der aktuell verwendete Rötelnvirus-Impfstamm (RA 27/3) führt - anders als andere, früher verwendete Impfstämme - auch (wie die Röteln-Erkrankung) zu einer Bildung von Röteln-Antikörpern an der Schleimhaut des Nasen-Rachen-Raumes.
-
Daher vermittelt dieser Impfstoff eine gewisse Herdenimmunität, die allerdings nicht vollständig ist, denn es gibt schon wenige Jahre nach der (initial erfolgreichen!) Impfung bei einem Teil der Geimpften die Gefahr der unbemerkten Reinfektion, die dann für andere ansteckend sein kann (Cusi 1993 und Cusi 1990).
-
Dieser Umstand konterkariert natürlich damit auch die Impfempfehlung für Jungen (die ja selber in aller Regel kein Komplikationsrisiko bei Röteln haben), da diese - bei nachlassender Immunität - auch geimpft die Erkrankung weitergeben können.
-
Eine Studie von 2023, die die Einführung der Windpocken-Impfung in Finnland begleitet hat, legt nahe, dass die Windpocken-Impfung einen gewissen Herden/Fremdschutz erzeugt: hier nahm auch die Inzidenz der Windpockenerkrankungen bei Säuglingen im ersten Lebensjahr deutlich ab ( IRR 0,13, 95% Vertrauensbereich 0,10 - 0,17, die entspricht einer Impfstoff-Wirksamkeit von 87%), obwohl das Alter für die erste Windpocken-Impfung erst bei 18 Monaten lag (Salo 2023).
-
Es bleibt natürlich die Frage offen, ob dieser Fremdschutz ein klinisch relevanter Effekt ist, wenn unverändert ein Großteil der europäischen Impfkommissionen nicht einmal einen Eigenschutz gegen Windpocken für sinnvoll halten und die langfristigen Folgen eines (Fremd-)Schutzes vor den Windpocken im Kindesalter (mögliche Verschiebung des Erkrankungsalters hin zu den Erwachsenen wie z.B. bei Mumps, Zunahme der Gürtelrose-Erkrankungen im Erwachsenenalter, ...) unverändert unklar sind.
-
eine 2020 veröffentlichte, vom Impfstoffhersteller gesponserte große Studie an über 24.000 australischen Jugendlichen konnte definitiv ausschließen, dass die MenB-Impfung eine Herdenimmunität vermittelt (Marshall 2020):
-
"Among Australian adolescents, the 4CMenB vaccine had no discernible effect on the carriage of disease-causing meningococci, including group B.“
-
“These results highlight the importance of individual vaccination for adequate protection, as the vaccine is unlikely to be able to stop spread of the bacteria between individuals.”
-
-
Hier ist die Situation widersprüchlich: trotz eines sehr niedrigen R0-Wertes von 1,3 (Trotter 2009 und 2005 - MenC sind nicht sehr ansteckend...) und damit einer für eine Herdenimmunität notwendigen bevölkerungsweiten Durchimpfungsrate von maximal 25% (Trotter 2009 und 2005) gibt es in Deutschland "keinen ausgeprägten Herdeneffekt" (RKI EpiBull 43/2016) - obwohl die Durchimpfungsrate z.B. bei Kindern im Grundschulalter in Deutschland fast 90% beträgt (RKI EpiBull 16/2016) - es fehle wahrscheinlich an einer hohen Durchimpfung z.B. der Jugendlichen, wie sie in anderen Ländern (z.B. GB) erreicht worden sei.
-
Die STIKO fasst zusammen: "Insgesamt sprechen diese Ergebnisse weiterhin vor allem für einen direkten Schutzeffekt der Impfung in den Altersgruppen mit hohen MenC-Impfquoten, aber noch nicht für einen ausgeprägten Herdenschutz." (RKI EpiBull 43/16) - und das zehn Jahre (!) nach Einführung der entsprechenden Imfempfehlung...
Eine durch Impfungen vermittelte Herdenimmunität
-
ist das klassische Argument für eine moralische oder sogar juristische Impfpflicht
-
ist aber keineswegs bei allen Impfungen überhaupt anzunehmen
-
ist keineswegs gleichbedeutend mit der „Herdenimmunität“ durch durchgemachte Erkrankungen – die dafür notwendigen Voraussetzungen erfüllt kein aktueller Impfstoff
-
kann daher als alleiniger Grund
-
weder das gesunde Überleben der zahlreichen Ungeimpften
-
noch die stabile epidemiologische Situation in Europa bei den auch impfpräventablen Erkrankungen erklären.
-
-
kann in einigen Fällen für die tatsächliche Bevölkerungsimmunität und Epidemiologie einzelner Erkrankungen auch negative Effekte haben.
Althouse BM. BMC Medicine 201513:146
Anderson RM. 1987. Epidemiol Infect. 99:65-84
Callender M. 2023. Front. Immunol. 14:1210580. doi: 10.3389/fimmu.2023.1210580
CDC. 2015. Epidemiology an Prevention of Vaccine-Preventable Diseases, 13th Edition/PinkBook. Measles. Abruf 19.07.2018
CDC 2010. MMWR 2010 Feb 12;59(5):125-9.
CDC. Pertussis FAQs. 2015.
CDC 2016. MMWR. July 29, 2016 / 65(29);731–734
CDU. https://www.cdu.de/system/tdf/media/dokumente/sonstige-beschluesse.pdf?file=1. Beschluss C 16, S. 4
Cortese MM. 2008.Clinc Infect Dis. 46:1172-1180
Cusi MG. 193. Arch Virol. 129:337-340
Cusi MG. 1990. Rossolini GM. Lancet. 336:1071
Dayan GH. N Engl J Med 2008; 358:1580-1589
Di Pietrantonj, C. 2021. DOI: 10.1002/14651858.CD004407.pub5.
Dittrich S. 2011. Vaccine. 29:9271-9275
Edwards D. 2018. Euro Surveill. 23(39):pii=1700681
Esposito S. 2019. Front. Immunol. 10:1344. doi: 10.3389/fimmu.2019.01344. Abruf 25.07.2019
Fanoy EB. 2011. Vaccine. 29:9551-9556
FDA. 2016. FDA Researchers Advance Science for Vaccines to Prevent Mumps and Whooping Cough. Abruf 22.02.2019
Fine PEM. Epidemiol Rev. 1993 Vol 15, No. 2:265-302
Fox JP. 1980. Rev Infect Dis. 2:277-81.
Gastañaduy PA. 2019. JAMA Pediatrics. doi:10.1001/jamapediatrics.2019.4357
GBE-Bund. Sterbefälle Tetanus. Abruf 07.08.2016
Glatman-Freedman A. 2012. Human Vaccines & Immunotherapeutics. 8(3):293–301
Marshall HS. 2020. N Eng J Med 382;4
Pappenheimer AM Jr.. Diphtheria. in: Germanier, R. Bacterial Vaccines. Berne. 1984
Plans-Rubió P. 2012. Preventive Medicine 55;72–77.
Quinlisk M. The Journal of Infectious Diseases 2010;202(5):655–656
RKI. 2020. Infektionsepidemiologisches Jahrbuch 2019.
RKI. 2014. RKI-Ratgeber - Masern. Abruf 19.07.2018
RKI. 2011. Epidemiologisches Bulletin. 2011(27):245–48
RKI. RKI-Ratgeber für Ärzte – Mumps. 2013
RKI. FAQs zu Poliomyelitis. Stand 10.09.2015
RKI. Impfquoten bei der Schuleingangsuntersuchung in D 2014. EpiBull 16/2016
RKI. Invasive Meningokokken-Erkrankungen 2012 – 2015. EpiBull 43/2016.
RKI. Diphtherie. 2009. Abruf 14.04.2017
Rota JS. 2009. J Med Virol. 81:1819-25
Salo H. 2023. https://doi.org/10.1016/j.vaccine.2023.09.024. Abruf 21.10.2023
Saragea M. Methods in Microbiology. 1979, Vol. 13, pp. 61-177.
Smith PG. Procedia in Vaccinology 2 (2010) 134–139
Strebel PM. Measles Vaccines in Plotkin S. Plotkin's Vaccines 7th ed. Philadelphia 2017
Trotter CL. Am. J. Epidemiol. (1 July 2005) 162 (1): 89-100. doi: 10.1093/aje/kwi160. Abruf 17.11.2016
Trotter CL. Expert Rev Vaccines. 2009;8(7):851-861.
Warfel JM. PNAS January 14, 2014
WHO. Recommendations for routine immunization. (Abruf 17.11.2016)
Eine umfassende Übersichtsarbeit zum diesem Thema können Sie - ausschließlich für den eigenen Bedarf! - hier herunterladen, hier finden Sie die Folien eines entsprechenden Vortrags, den ich im Februar 2018 auf dem Impfkongress der "Ärzte für individuelle Impfentscheidung eV" in Berlin gehalten habe.