Ein kurzer Abriss über Pockenimpfstoffe
Vakzinia-Immunglobulin wurde vor allem zur Behandlung von Impfkomplikationen nach der Pockenimpfung eingesetzt, z.B. bei Ekzema vakzinatum. Trotz großflächiger Anwendung liegen keine methodisch belastbaren Studien zur Wirksamkeit vor (Kennedy 2018).
Historisch beschrieben schon ab etwa 1000 v. Chr. beschriebene Inokulation infektiösen Materials in die Haut oder die Nase (so genannte Variolation) - was zu einem wesentlich milderen Verlauf führte, als die typische Infektion über die Atemwege und Immunität vermittelte.
Anfang des 19. Jahrhunderts verwendete Edward Jenner initial Kuhpocken-Viren. Laborexperimente führten auf bis heute nicht vollständig geklärtem Weg (Kennedy 2018) zum Vaccinia-Virus, einem eigenständigen Orthopox-Virus, das Immunität gegen die echten Pocken vermittelt und in der Natur nicht vorkommt (so genannte Vaccination).
Experimente mit inaktivierten Pockenimpfstoffen (Nicht-Lebendimpfstoffe) führten zwar zu hohen Titern neutralisierender Antikörper, aber zu keinem klinischen Schutz vor der Erkrankung (Amies 1961).
Verwendet wurden für die Lebend-Impfstoffe initial moderat abgeschwächte Vaccinia-Stämme (Lister/NYCBHO/EM-63/MVA u.a.) als so genannte Pockenimpfstoffe der ersten Generation.
Aktuelle Pockenimpfstoffe
zweite Generation - vermehrungsfähige Impfviren
- ACAM2000 von Sanofi Pasteur, basiert auf NYCBOH-Stamm, lyophilisiertes reines Virus, muss vor Anwendung rekonstituiert werden
dritte Generation - nicht-vermehrungsfähige Impfviren
- Imvamune/Imvanex® von Bavarian Nordic, basiert auf MVA-Stamm, tiefgefrorene Suspension; gefriergetrocknete Version in Entwicklung.
- Auch von der EMA zugelassen, allerdings "unter besonderen Umständen":
"This medicine was authorised under exceptional circumstances, because the applicant was unable to provide comprehensive data on the efficacy and safety of the medicine under normal conditions of use. This can happen because the condition to be treated is rare or because collection of full information is not possible or is unethical." (EMA 2022)
-
Die Zulassung beruht auf reinen Serokonversions-Studien, d.h. auf der Messung von Antikörpern im Blut der Geimpften (Pittman 2019) - der Beweis eines Schutzes vor der Erkrankung am Menschen steht noch aus. "The European Medicines Agency considered that Imvanex is effective at triggering the production of antibodies against smallpox to a level that provides protection at least as high as that from conventional smallpox vaccines. However, the duration of protection is not known." (EMA 2022). Und: "Efficacy data of the currently available smallpox vaccine(s) against MPX are lacking, and safety data for the useof the smallpox vaccine in young children, pregnant women and immunocompromised are also lacking" (ECDC 2022). Allerdings sind die Tierversuchsstudien, die eine hohe Schutzwirkung auch vor der Erkrankung zeigten, sämtlichst mit Affenpocken durchgeführt wurden, da aus Sicherheitsgründen Experimente mit Pockenviren im Rahmen von Arzneimittelstudien nicht möglich sind (UKHSA 2022).
-
Veröffentlichte Studien mit Kindern, an Schwangeren oder Stillenden existieren nicht ("The safety and efficacy of IMVANEX in children below 18 years have not been established." EMA 2022) - die EMA rät, die Anwendung in Schwangerschaft und Stillzeit zu vermeiden, es sei denn, die Gefahr einer Pocken- (nicht Affenpocken) Infektion sei groß.
-
Der Impfstoff ist in der EU als Impfstoff gegen Pocken, nicht aber gegen Affenpocken zugelassen - in den USA hat die FDA die Zulassung 2019 auf Affenpocken erweitert (FDA 2019, Präparat heißt dort Jynneos®).
-
Nach Angaben von Hersteller und EMA ist das im Impfstoff verwendete Virus nicht mehr vermehrungs- und ansteckungsfähig, kann also auch nicht mehr auf Kontaktpersonen übertragen werden. "The vaccinia virus in Imvanex cannot replicate in human cells and hence is less likely to cause side effects than conventional smallpox vaccines." (EMA 2022)
- Auch von der EMA zugelassen, allerdings "unter besonderen Umständen":
Mittlerweile sind auch Impfstoffe der "vierten Generation" in Entwicklung, die nur noch auf Teilen des Pockenvirus beruhen und auf Protein- oder DNA-Technologie basieren.
Anwendung
Typisch mit gegabelter Nadel, zwischen deren beiden Enden sich der Impfstoff befindet (CDC-Video hier).
Imvanex® wird regulär subcutan injiziert.
Typische Impfreaktion
An der Impfstelle entsteht innerhalb weniger Tage typischerweise ein Knötchen, das sich über eine Blase und eine Pustel zur Kruste verwandelt und nach Abfallen derselben eine typische Impfnarbe hinterlässt.
Immunologisch entstehen Antikörper etwa 10 Tage nach der Impfung, eine zelluläre Immunität schon nach 5 - 6 Tagen - damit ist die Reaktion auf das Vaccinia-Virus schneller als die auf das echte Pockenvirus, was eine aktive Impfung in den ersten Tagen nach einer vermuteten Ansteckung erlaubt.
Da die entstehende Immunität nicht zuverlässig messbar ist, wurde das Entstehen der typischen Blase an der Impfstelle ("vaccine take") als Zeichen einer erfolgreichen Impfung gewertet. Die entstehenden Hautveränderungen sind bis zum Entstehen der Kruste grundsätzlich ansteckend.
Nach Anwendung einiger europäischer Vaccinia-Stämme ließ sich das Impfvirus nach der Impfung im Rachenabstrich nachweisen.
Typische Nebenwirkungen der Pockenimpfung sind:
-
Ansteckung anderer durch Kontakt zu Impfstelle
-
Geschwürbildung an der Impfstelle ("progressive vaccinia")
-
Ausbreitung der Impfreaktion, u.U. auf den gesamten Körper (Ekzema vakzinatum)
-
Herzmuskelentzündung
-
Enzephalitis/Hirnentzündung
Eine Meta-Analyse der historischen US-amerikanischen Impfkampagnen der 1960er- und 70er-Jahre nennt hier folgende Häufigkeiten pro eine Million Geimpfter:
- 60 Fälle von Ansteckung anderer, 40 von generalisierter Vaccinia-Ausbreitung, 13 von Ekzema vakzinatum, 3 Enzephalitis-Fälle (Aragón 2003)
Die US-amerikanischen CDC gehen von einer Häufigkeit lebensbedrohlicher Nebenwirkungen von bis zu 1/20.000 aus (CDC).
Eine Analyse der neueren Impfkampagnen Anfang der 2000er-Jahre ergab bei knapp 40.000 Geimpften eine Häufigkeit schwerer Nebenwirkungen von 217/10.000, darunter 10 lebensbedrohliche Ereignisse und 3 Todesfälle (Casey 2005).
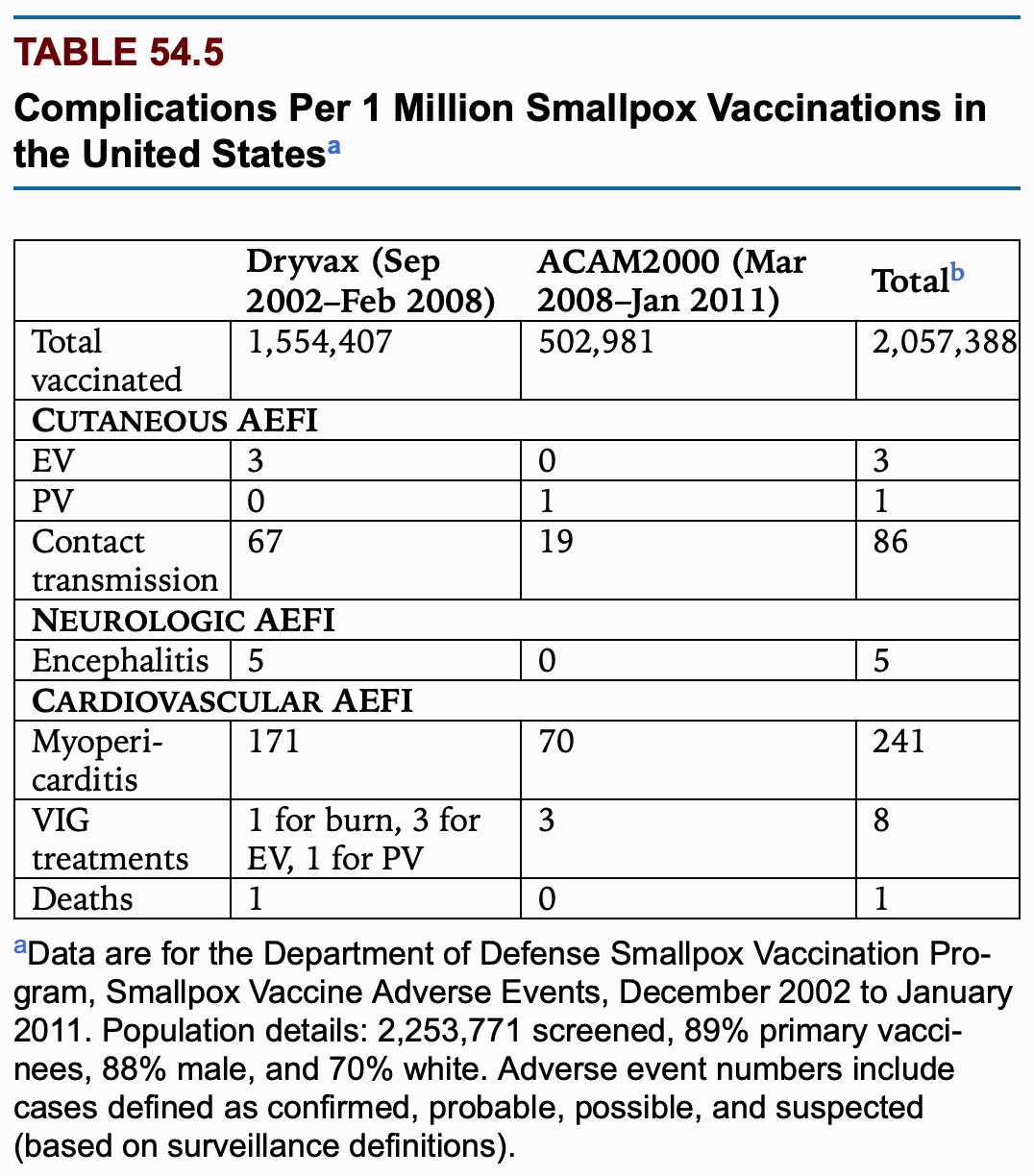
Die Untersuchung großangelegter Impfkampagnen im US-amerikanischen Militär ergab folgende Daten (Kennedy 2018)
Amies CR. 1961. Can J Microbiol 1961;7:141-52
Aragon TJ. Risks of serious complications and death from smallpox vaccination: A systematic review of the United States experience, 1963–1968. BMC Public Health 3, 26 (2003). https://doi.org/10.1186/1471-2458-3-26
Casey CG. 2005. Adverse Events Associated With Smallpox Vaccination in the United States, January-October 2003. JAMA. 2005;294(21):2734–2743. doi:10.1001/jama.294.21.2734
CDC. Side-effects of smallpox-vaccination. Abruf 22.05.2022
ECDC. 2022. Risk assessment: Monkeypox multi-country outbreak. Abruf 23.05.2022
EMA. 2022. Imvanex. Abruf 22.05.2022
FDA. 2019. Jynneos. Abruf 23.05.2022
Kennedy RB. Smallpox and Vaccinia. Vaccines, 7th edition
Pittman PR. 2019. N Engl J Med 381(20):1897-1908. doi: 10.1056/NEJMoa1817307.
UKHSA. 2022. Monkeypox vaccination. Abruf 23.02.2022