Nicht erst seit dem Ende der Coronoia sind - auch kurzfristig geplante - Fernreisen auch mit Kindern (wieder) en vogue. In vielen (Fern-)Reiseländern besteht unverändert ein Risiko, an Tollwut zu erkranken, einer Erkrankung, die - einmal ausgebrochen - immer tödlich verläuft. Lesen Sie hier, was Sie über Erreger, Ansteckung und Erkrankung wissen sollten.
Erreger der Tollwut sind so genannte Lyssaviren, von denen wiederum fast 20 verschiedene Unterarten unterschieden werden.
Grundsätzlich sind alle Säugetiere mögliche Träger dieser Viren, in der Praxis spielen jedoch vor allem fleischfressende Säugetiere und Fledertiere für die Übertragung der Tollwut eine Rolle. 99% der menschlichen Tollwutfälle werden durch Hunde oder Katzen übertragen, Affen sind als Überträger selten, menschliche Todesfälle durch Übertragung von Affen außerhalb Brasiliens "Raritäten" (RKI 2023). Die früher auch in Deutschland empfohlene Impfung z.B. nach einem Biss durch (wild lebende) Nagetiere wird mittlerweile von der WHO weltweit nicht mehr empfohlen (WHO 2018).
Die Übertragung der Tollwut auf den Menschen erfolgt in der Regel durch den Speichel des infektiösen Tieres, entweder durch Bissverletzung oder durch Wund- oder Schleimhautkontakt. Eine Infektion über virushaltige Aerosole ist (z.B. in Viruslabors) theoretisch möglich, aber extrem selten.
Andere Übertragungsformen sind dokumentiert, aber Raritäten: so wurden weltweit immer wieder Tollwut-Erkrankungen dokumentiert, die durch unvollständig inaktivierten Tollwut-Impfstoff ausgelöst wurden (s. dazu hier). Ein Todesfall bei einem Vater beruhte darauf, dass dieser die Bissverletzung seines Kindes "aussaugte" - das Kind wurde behandelt und überlebte, der Vater wurde nicht behandelt (er war ja nicht gebissen worden...) und verstarb... (Gibbons 2002)
Je nach Art und Intensität des Kontaktes werden hier verschiedene "Expositionsgrade" unterschieden, die für das medizinische Vorgehen im möglichen Infektionsfall von Bedeutung sind:
Ohne so genannte Postexpositionsprophylaxe (also die Schutzimpfung nach einer Bissverletzung) beträgt das Risiko, an Tollwut zu erkranken, nach dem Biss durch ein tollwutinfektiöses Tier bei Bissen im Kopfbereich > 50%, am Stamm 9%, an Armen und Händen 22% und an den Beinen etwa 12% (Shim 2009).
Bei der Immunologie der Tollwut ist noch vieles unverstanden: so ist nicht abschließend geklärt, wie denn die auf die Impfungen hin entstehenden Serum-Antikörper das Virus bekämpfen (unstrittig ist, dass sie es tun). Auch warum nicht wenige der Tollwut-Erkrankten keine Antikörper-Reaktion gegen das Virus bilden ist so wenig abschließend geklärt wie die Frage, ob die Immunreaktion auf das Wildvirus (nicht etwa: die Impfung) unter Umständen für einen Teil der Krankheitssymptomatik verantwortlich ist. Bei Erkrankten sind Antikörper in der Regel erst mit dem Beginn der neurologischen Symptomatik nachweisbar - im Gegenzug gibt es durchaus Menschen, die ohne Tollwut-Vorgeschichte nachweisbare Antikörperspiegel aufweisen. (Rupprecht 2022)
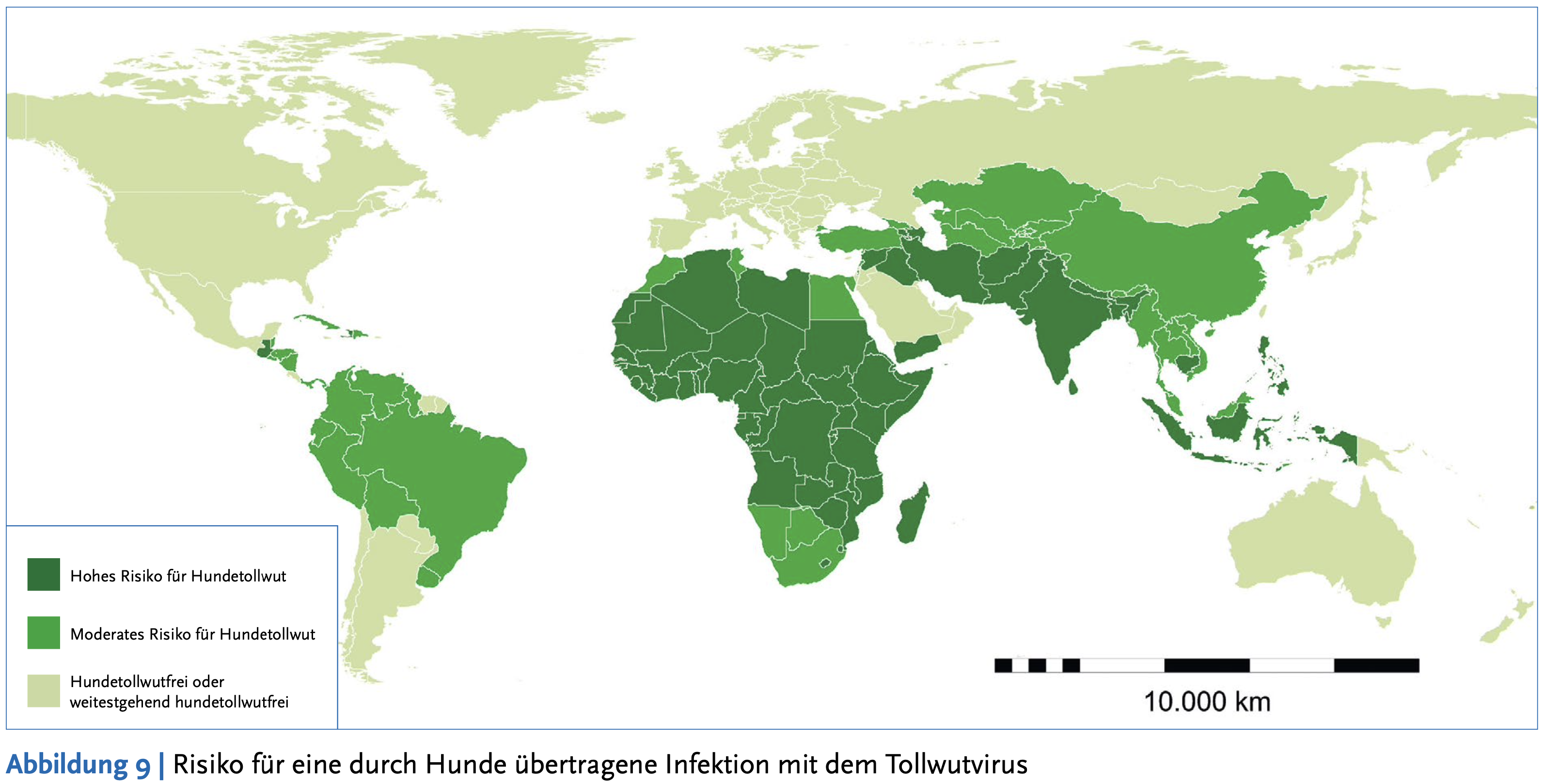
Grundsätzlich ist die Tollwut als Erkrankung weltweit verbreitet, die meisten menschlichen Todesfälle treten jedoch in Asien (fast 60%) und Afrika (gut 36%) auf. Etwa 40% der weltweit Erkrankten sind Kinder und Jugendliche unter 15 Jahren (WHO 2018).
Westeuropa und Nordamerika (inklusive Mexiko) gelten mittlerweile als frei von so genannter "terrestrischer Tollwut", also von Tollwut-Erkrankungen, die durch Hunde übertragen werden.
Die "nicht-terrestrische" Tollwut bei Fledertieren ist auch in Deutschland und Europa unverändert ein (geringes) Risiko, Erkrankungen auch beim Menschen sind als Einzelfälle immer wieder dokumentiert (RKI 2003).
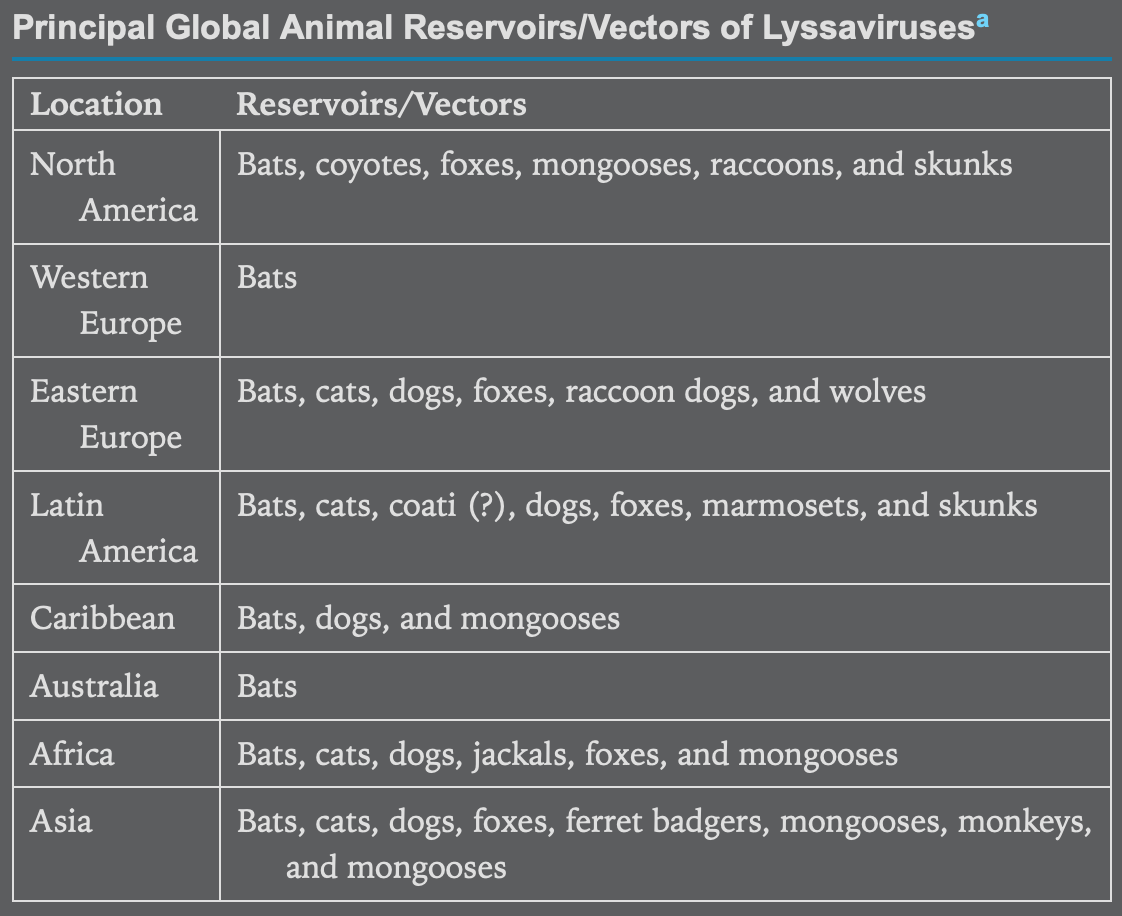
Eine Übersicht über die aktuell relevanten Vektoren weltweit findet sich bei Rupprecht (Rupprecht 2022).
Die Inkubationszeit zwischen Tierkontakt und Krankheitsausbruch schwankt stark - sie beträgt im Mittel 2 - 3 Monate, kann in seltenen Fällen aber auch nur wenige Tage oder mehrere Jahre betragen. Da das Tollwutvirus nach dem Eindringen in den menschlichen Körper entlang der peripheren Nervenbahnen in Richtung des zentralen Nervensystems aufsteigt, sind bei Eintrittspforten am Kopf oder an stark mit Nerven versorgten Körperstellen (Hände) kürzere Inkubationszeiten beschrieben (RKI 2022).
Nach einem unspezifischen Prodromalstadium mit grippaler Symptomatik kommt es in 80% der Fälle zum Krankheitsbild einer hirnstammbetonten Hirnentzündung (Enzephalitis) mit Bewusstseinsstörungen, Krampfanfällen und Wesensveränderungen. In 20% der Fälle kommt es zum so genannten paralytischen Verlauf mit Missempfindungen an Armen und Beinen und zunehmender Muskelschwäche.
Es kommt im Verlauf zu einer Hirnstammfunktionsstörung (Koma, Atemlähmung) und zum Tod nach etwa 7 - 10 Tagen.
Eine ursächliche Behandlung gibt es nicht, die Tollwut-Erkrankung führt nach Krankheitsausbruch unweigerlich zum Tod. (Weltweit wurden bislang weniger als 20 Fälle dokumentiert, in denen eine Tollwut-Erkrankung (mit schweren Folgeschäden) überlebt wurde (Jackson 2017).
Gibbons RV. 2002. Cryptogenic rabies, bats, and the question of aerosol transmission. Ann Emerg Med. 2002;39:528–536
Jackson AC. 2017. Curr Infect Dis Rep. 2017;18(11).
RKI. 2023. EpiBull 14/23.
RKI. 2022. Merkblätter Tollwut. https://www.rki.de/DE/Content/Infekt/EpidBull/Merkblaetter/Ratgeber_Tollwut.html. Abruf 11.10.2023
RKI. 2003. EpiBull 26/03.
Rupprecht CE. Lyssavirusses and Rabies Vaccines. in: Plotkin's Vaccines 8th edition. Elsevier 2022.
Shim E. 2009. Vaccine. 2009; 27(51),:7167–7172.
WHO. 2018. World Health Organization: WHO Expert Consultation on Rabies, third report. Geneva: World Health Organization. 2018 (WHO Technical Report Series, No. 1012). apps.who.int/iris/ handle/10665/272364