Neben der notwendigen Zahl der Masern-Impfdosen (s. hier) wird auch deren Zeitpunkt sowohl international als auch sogar zwischen verschiedenen deutschen Impfkommissionen hochkontrovers diskutiert.
Die Sterblichkeit an Masern war, auch vor der Einführung der Masernimpfung, im ersten Lebensjahr verglichen mit anderen Lebensphasen relativ am höchsten - dennoch ging diese Sterblichkeit im Säuglingsalter nach der Impfempfehlung für Masern relativ am wenigsten stark zurück (Shanks 2015, Engelhardt 1980, Barkin 1975).
Masern gehören zu den klassischen Erkrankungen mit einem Nestschutz junger Säuglinge durch Antikörper der Mutter, die gegen Ende der Schwangerschaft durch die Plazenta auf den Säugling übertragen werden. Diese vermitteln einen gewissen (unvollständigen) Schutz des Säuglings selber, verhindern aber in den ersten Lebensmonaten eben auch eine effektive Impfung gegen Masern, indem sie die Impfviren neutralisieren (so genanntes blunting). Viele der Studien zur Masernimpfung bei Säuglingen stammen noch aus den 60er-, 70er- und 80er-Jahren des vergangenen Jahrhunderts, wurden also bei Kindern erhoben, deren Mütter keine Impfimmunität, sondern die wesentlich effektivere Immunität nach überstandener Masernerkrankung weitergaben - aktuellere Studien aus diesem Jahrhundert finden hier, dass im Alter von 6 Monaten mittlerweile 99% der Kinder geimpfter Mütter und 95% der Kinder von Müttern mit Masern in der Vorgeschichte keine nachweisbaren mütterlichen Antikörper mehr aufweisen (Leuridan 2010). Durch die in vielen Ländern de facto erreichte Elimination der Masern werden auch Antikörper-Spiegel von Müttern mit Masern in der Vorgeschichte nicht mehr aufgefrischt, was auch hier zu einem schlechteren Nestschutz führt (Wang 2023). Somit führt die Masernimpfung und die Eliminationsstrategie der WHO auch zu einem schlechteren (Nest-)Schutz der durch schwere Verläufe besonders gefährdeten Säuglinge (Carson 1995) - ein Kollateralschaden der Masernimpfempfehlung, der auch der STIKO bekannt ist(Löll 2011). Eine chinesische Studie aus dem Jahr 2023 geht davon aus, dass im Mittel im Alter von etwa 10 Wochen kein schützender Antikörper-Spiegel durch den Nestschutz mehr zu erwarten ist (Wang 2023).
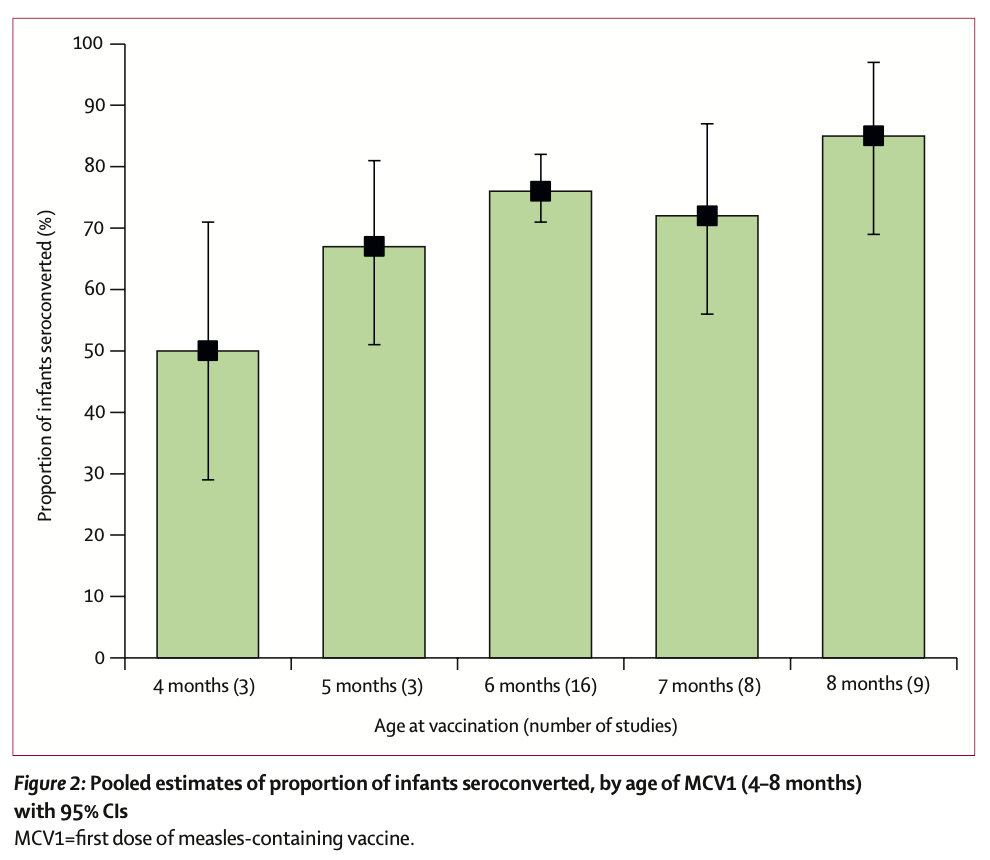
Daher wird immer wieder ausgelotet, wie früh eine erste Masernimpfung (MCV1) denn sinnvoll möglich ist, um junge Säuglinge nachhaltig zu schützen - und hier zeigen sich deutliche Grenzen, wie die Serokonversionsquoten (also der Anteil der Kinder mit einer erfolgreichen Antikörperbildung) nach Impfung aus einer großen Meta-Analyse zeigen (Nic Lochlainnen 2019):
Eine MCV1 im Alter von 4 Monaten führt nur bei etwa 50% der Kinder zu schützenden Antikörpern, im Alter von 8 Monaten sind es immerhin schon 85% - nach dem ersten Geburtstag sind es dann ≥ 95% (Nic Lochlainn 2019, Strebel 2018). Auch die Höhe der entstehenden Antikörperspiegel war bei einer MCV1 vor dem 9. Lebensmonat im Mittel nur etwa halb so hoch wie bei einer MCV1 ab dem 9. Lebensmonat. Die zelluläre Immunantwort scheint durch eine frühe MCV1 nicht beeinträchtigt zu sein (Nic Lochlainn 2019).
Auch in der klinischen Effektivität der Impfung zeigt sich dieser Unterschied: die Impfstoff-Effektivität im Schutz vor Masern liegt einer großen Metaanalyse zu Folge bei einer MCV1 vor dem 9. Lebensmonat deutlich unter 60%, danach dann über 80% (Nic Lochlainn 2019).
Trotz dieses früheren und stärkeren Rückgangs mütterlicher Antikörper bei jungen Säuglingen bleibt die Erstimpfung im ersten Lebensjahr auch in epidemiologischen Untersuchungen ein Hauptrisikofaktor für das primäre oder sekundäre Impfversagen:
So zeigt die Analyse einer großen kanadischen Epidemie der 90er-Jahre: "Children who received their first dose of measles vaccine at 11 months of age and their second dose after age 12 months had a significantly greater risk of measles than those who received both doses after their first birthday (OR, 3.2)" - und die Autoren fassen zusammen: "Longterm protection against measles in children vaccinated in early infancy (< 12 months old) is unclear." (de Serres 1999).
Dies bestätigt sich in einer chinesischen Studie aus dem Jahr 2023: bei einer MCV1 im Alter von 8 und einer MCV2 im Alter von 18 Monaten sind den Autoren zu Folge schon im Alter von 14 Jahren keine schützenden Antikörper-Spiegel mehr zu erwarten (Wang 2023).
Und auch die Analyse der deutschen KIGGs-Erhebung des RKI aus diesem Jahrhundert zeigte [Hervorhebung von mir]: "Seronegativity was more likely in children who had received the first measles vaccination during their first year of life than in children who had received the first dose after the first year of life. The odds of being seronegative after early vaccination was 2.86 (95% CI 1.64-3.19) for a single dose and was 2.29 (95% CI 1.64-3.19) for two-dose vaccination. ...Our large, representative study showed inferior immune responses in children who were very young age at first vaccination (even if a second vaccination was given at older age). Children who received their first vaccination within the first 12 months of life exceeded the target of less than 5% seronegativity even if they had a second dose at older ages. ... These results indicate that mispriming of the immune system after early vaccination cannot be cured by a late second dose of MCV." (Poethko-Müller 2011).
Dieses Ergebnis - vor allem auch die Nicht-Reparierbarkeit des durch die frühe Erstimpfung entstehenden schlechteren Schutzes - finden auch andere Autoren: "...antibody responses among children born to vaccinated mothers were reduced based on earlier administration of their first measles vaccine dose at ≤12 versus ≥15 months of age. Negative effects of earlier age at first measles vaccine dose persisted after the second dose." (Carazo Perez 2017).
Bei einer Impfung vor dem ersten Geburtstag bilden aber nicht nur weniger geimpfte Kinder ausreichend hohe Antikörperspiegel, die Antikörper sind auch qualitativ weniger wirksam, ihre "Avidität" (Bindungs- und damit Neutralisationsfähigkeit für Masernviren) und damit der entstehende Schutz ist schlechter (WHO 2017): und zwar bei einer MCV1 im Alter von 6 Monaten schlechter als bei einer im Alter von 9 Monaten und bei dieser schlechter als bei Erstimpfung im Alter von 12 Monaten (Nic Lochlainnen 2019).
Eine Meta-Analyse aus dem Jahr 2020 bestätigt beide Befunde: "Earlier age at MCV1 decreases measles protection and immunogenicity after one dose and might still have an impact on vaccine failures after two doses of measles vaccine." (Carazo 2020).
Selbst die WHO musste auf einem informellen Expertentreffen im Jahr 2025 einräumen, dass das Problem des schnelleren Nachlassens der Impfimmunität nach einer frühen ersten Masernimpfung langfristig zu einer Verschlechterung der Bevölkerungsimmunität führen kann (Varma 2025).
Zusammengefasst führt also eine erste Masernimpfung vor dem ersten Geburtstag:
-
bei einem deutlich geringeren Teil der geimpften Kinder zur Bildung ausreichend hoher Antikörperspiegel
-
zur Bildung qualitativ schlechter wirksamer Antikörper
-
damit zu einem (vermutlich lebenslang) schlechteren Schutz vor Masern, der im Nachhinein nicht mehr korrigiert werden kann.
Bei der Wahl des "richtigen" Impfzeitpunkts stehen also zwei Aspekte einander gegenüber:
die besondere (und durch den immer geringer werdenden Nestschutz zunehmende) Gefährdung der Säuglinge, die für eine möglichst frühe Impfung spricht auf der einen und das Wissen um die schlechtere Wirksamkeit (und die Verschlechterung der Masern-Immunität u.U. für den Rest des Lebens) der Impfung vor dem ersten Geburtstag auf der anderen Seite.
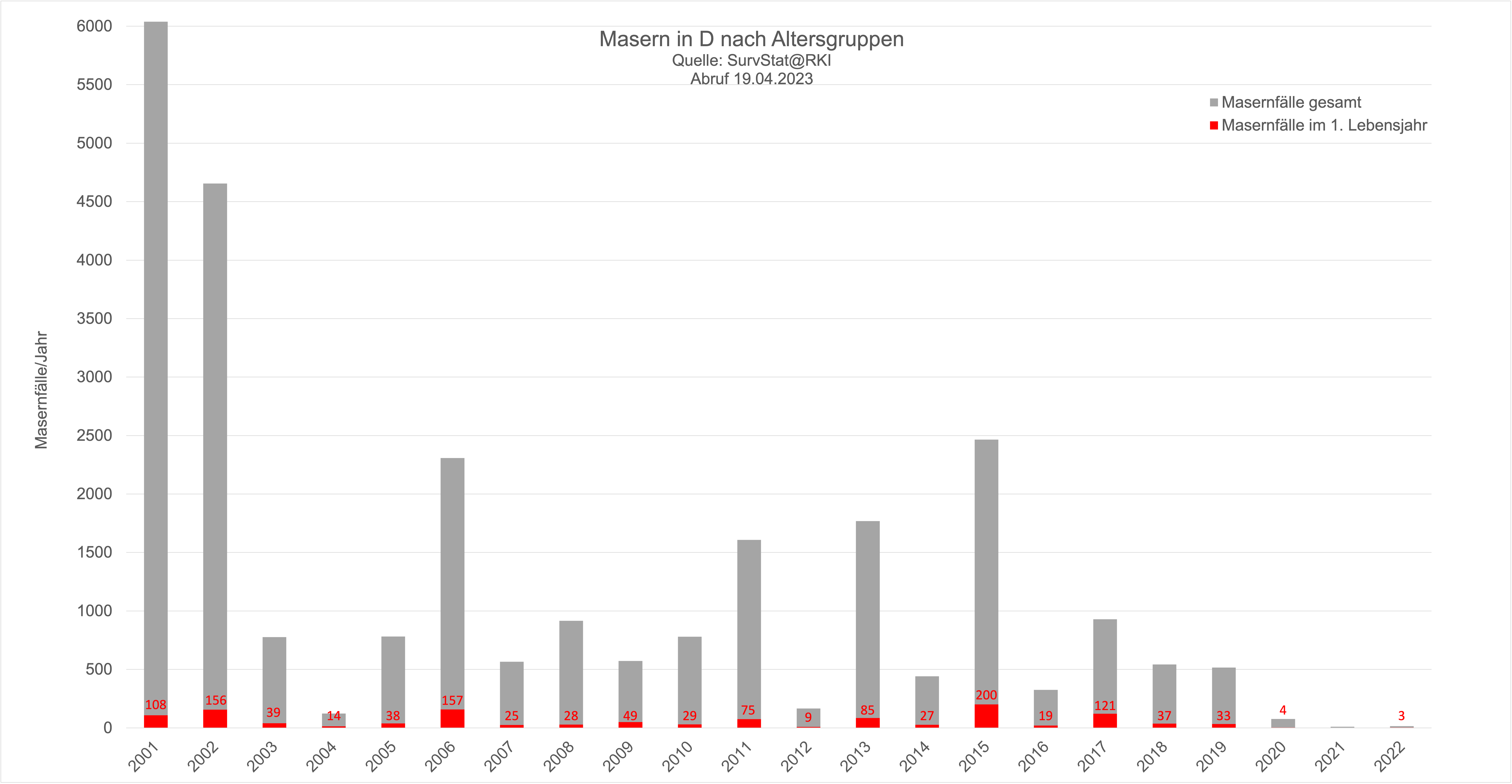
Dieses Dilemma sieht auch z.B. die WHO und empfiehlt die Impfung im Alter von 9 Monaten für diejenigen Länder, "in which the risk of measles mortality among infants remains high" (WHO 2017). Nachdem in Deutschland seit 1993 kein Säugling mehr an Masern gestorben ist (www.gbe-bund.de - Sterbefälle), trifft dies auf Deutschland definitiv nicht zu. Auch die Zahl der Masernfälle im ersten Lebensjahr verglichen mit der Gesamtzahl der Fälle zeigt deutlich, dass Säuglingsmasern in Deutschland kein dramatisches Problem sind:
Damit gilt in Deutschland: "In countries with low levels of measles transmission (i.e. those nearing measles elimination or verified as having eliminated endemic measles virus transmission) and therefore the risk of measles virus infection among infants is low, MCV1 may be administered at 12 months of age to take advantage of the higher seroconversion rates achieved at this age." (WHO 2017).
Angesichts der epidemiologischen Situation in Deutschland und dieser Empfehlung der WHO (der außer Deutschland praktisch alle vergleichbaren europäischen Nachbarländer folgen) ist die Entscheidung der STIKO, die erste Masernimpfung ab dem 11. Lebensmonat, für Krippenkinder schon ab dem 9. Lebensmonat zu empfehlen und damit die oben aufgeführten, erheblichen Nachteile in Kauf zu nehmen, nicht nachvollziehbar.
Eine MCV1 zwischen dem ersten Geburtstag und dem Alter von 15 Monaten wird der Masern-Situation in Deutschland und dem Bestreben eines möglichst optimalen Impfschutzes sicher besser gerecht. Hinweise, dass ein noch späterer Impfbeginn weitere Vorteile brächte, sind nicht konsistent, die oben schon zitierte kanadische Analyse fand: "As expected, the protection induced by a single dose of vaccine increased with older age at vaccination but reached a plateau at age 15 months." (de Serres 1999). Demgegenüber findet eine italienische Studie von 2019, dass die Dauer des Impfschutzes (gemessen über den Antikörperspiegel) bei einer Impfung ab dem zweiten Geburtstag noch einmal signifikant zunimmt, verglichen mit Erstimpfungen bis zum 15. oder zwischen dem 16. und 23. Lebensmonat (Bianchi 2019).
Da der letzendliche Grund für die zweite Masernimpfung ja nicht die Verbesserung des Impfschutzes bereits Maserngeimpfter ist (das leistet sie nicht nennenswert, s. hier), sondern epidemiologische Überlegungen, orientiert sich ihr Zeitpunkt auch oft an den dementsprechenden Rahmenbedingungen wie z.B. den etablierten Vorsorge- oder Schuluntersuchungen eines Landes.
Lässt sich also aus der Sicht des Impfschutzes für das einzelne Kind die deutsche Aufgeregtheit um die Notwendigkeit der zweiten Masernimpfung schon nicht nachvollziehen, so gilt dies umso mehr für den deutschen Sonderweg, diese dann auch noch zu einem so frühen Zeitpunkt zu empfehlen. Außer Österreich, Liechtenstein und Luxemburg empfiehlt kein anderes europäisches Land die MCV2 so früh wie die STIKO (mit 15 Monaten - nicht wenige Länder empfehlen zu diesem Zeitpunkt gerade einmal die MCV1...). Immerhin 13 von 31 von der Europäischen Gesundheitsbehörde ECDC erfassten Länder der erweiterten EU empfehlen die MCV2 ganz regulär erst nach dem 6. Geburtstag.
Auch die nicht wirklich impfkritische WHO empfiehlt für ein Land wie Deutschland (MCV1-Durchimpfung > 90% und Schulbesuch bei > 95% der Kinder) die Gabe der MCV 2 im Schulalter: "If MCV1 coverage is high (>90%) and school enrolment is high (>95%), administration of routine MCV2 at school entry may prove an effective strategy for achieving high coverage and preventing outbreaks in schools" (WHO 2017).
Besonders interessant ist in diesem Zusammenhang, dass die SIKO, also die Sächsische Impfkommission, sich ausdrücklich zu diesem von der WHO empfohlenen späteren Zeitpunkt der MCV2 bekennt, diese Empfehlung ausführlich wissenschaftlich fundiert und die STIKO für ihre - so wörtlich - "Vorverlegung ... ohne wissenschaftliche Begründung" unverblümt kritisiert (Beier 2017). Die vom BGH ja als "medizinischer Standard" apostrophierte Impfempfehlung der STIKO ist also nicht einmal unter den deutschen Gesundheitsbehörden unumstritten... .
Barkin RM. 1975. Am J Epid. 102:341–349
Beier D. SIKO aktualisiert Impfempfehlungen bei Masern-Mumps-Röteln, Influenza, Hepatitis B und HPV. KVS-Mitteilung Heft 2/2017. Abruf 07.04.2019
Bianchi FP. 2019. J Infect Dis. 2019 Oct 3. pii: jiz508. doi: 10.1093/infdis/jiz508. Abruf 07.10.2019
Carazo S. 2020. https://doi.org/10.1186/s12879-020-4870-x
Carazo Peres S. 2017. Clin Infect Dis. 2017 Oct 1;65(7):1094-1102. doi: 10.1093/cid/cix510.
Carson MM. 1995. Pediatr Infect Dis J.14:17–22.
De Serres G. 1999. J Infect Dis. 180(1):187–90
Leuridan E. 2010. BMJ. 340:c1626
Löll C. 2011. Masern auf dem Weg zur Erwachsenen-Krankheit. Die Welt 25.10.2011. Abruf 30.03.2019
Nic Lochlainn LM. 2019. https://doi.org/10.1016/S1473-3099(19)30395-0
Poethko-Müller C. 2011. Vaccine, 29 (45), pp. 7949-7959.
Strebel PM. Measles Vaccines in Plotkin S. Plotkin's Vaccines 7th ed. Philadelphia 2017
Wang Q. 2023. https://doi.org/10.1038/s41467-023-37407-x
Varma A. 2025. https://doi.org/10.1016/j.vaccine.2025.127187
WHO. 2017. WER. 92:205–228